题目内容
一定量的质量分数为14%的KOH溶液,若蒸发掉100 g水后,其质量分数变为28%,体积为125 mL,且蒸发过程中无晶体析出,则浓缩后的KOH溶液的物质的量浓度为( )
| A.2.2 mol·L-1 | B.4 mol·L-1 |
| C.5 mol·L-1 | D.6.25 mol·L-1 |
B
设蒸发后溶液的质量是x。由于蒸发过程中溶质是不变的,所以(x+100)×14%=x×28%,解得x=100g,所以含有的溶质是28g,物质的量是0.5mol,则浓度是0.5mol÷0.125L=4mol/L,答案选B。

练习册系列答案
相关题目

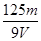 mol/L
mol/L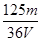 mol/L
mol/L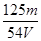 mol/L
mol/L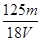 mol/L
mol/L