题目内容
【题目】海洋是一座巨大的化学资源宝库,从中可以提取许多常见的化学物质,结合所学知识回答下列问题,
(1)“吹出法”提溴空气吹出法是工业规模提溴的常用方法,其流程如下:

其中步骤②~④的目的是________________________________________________。步骤③反应的离子方程式为_______________________________________________。除SO2外,步骤③还可以选用Na2CO3溶液吸收溴,主要反应是Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3(未配平),吸收1molBr2时,转移电子的物质的量为__________________mol。
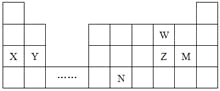
(2)实验室模拟从海带中提取碘,可能经历如下操作(或过程),请选择必要的操作(或过程),并按实验的先后顺序排列________________________________________________(填写编号)

仪器X的名称__________________,将X中的液体分离的具体操作为:打开X上端玻璃塞,_______________________________________________________________________________。
(3)卤块的主要成分是MgCl2,此外还含Fe2+、Fe3+和Mn2+等杂质离子。现以卤块为原料按下图流程制备轻质氧化镁,若要求产品尽量不含杂质,而且生产成本较低,请根据表1和表2提供的资料,回答下列问题:

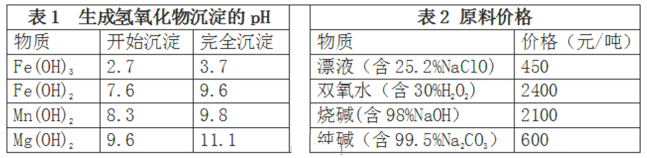
已知:Fe2+氢氧化物呈絮状,不易从溶液中除去。
步骤①反应的离子方程式为:___________________________________________________;
步骤②的反应方程式为:_______________________________________________________。
【答案】富集溴元素(或提高溴水浓度,意思正确可得分) SO2+Br2+2H2O=4H++SO42-+2Br-![]() CEAD分液漏斗再打开分液漏斗活塞,使下层液体从下口放出,待下层液体刚好放出时,关闭分液漏斗活塞,再从上口将上层液体倒出ClO-+2H++2Fe2+=2Fe3++Cl-+H2OMgCO3+H2O
CEAD分液漏斗再打开分液漏斗活塞,使下层液体从下口放出,待下层液体刚好放出时,关闭分液漏斗活塞,再从上口将上层液体倒出ClO-+2H++2Fe2+=2Fe3++Cl-+H2OMgCO3+H2O![]() Mg(OH)2+CO2↑
Mg(OH)2+CO2↑
【解析】
(1) 氧化后的海水虽然含有溴单质,但浓度低,如果直接蒸馏原料,生产成本高。“空气吹出、![]() 吸收、氧化”的过程实际上是一个
吸收、氧化”的过程实际上是一个![]() 的浓缩过程;Na2CO3溶液吸收溴反应配平可得:3Br2+6Na2CO3+3H2O=5NaBr+NaBrO3+6NaHCO3,其中溴与转移的电子的关系为:3 Br2——5e-,故答案为:富集溴元素(或提高溴水浓度,意思正确可得分)、SO2+Br2+2H2O=4H++SO42-+2Br-、
的浓缩过程;Na2CO3溶液吸收溴反应配平可得:3Br2+6Na2CO3+3H2O=5NaBr+NaBrO3+6NaHCO3,其中溴与转移的电子的关系为:3 Br2——5e-,故答案为:富集溴元素(或提高溴水浓度,意思正确可得分)、SO2+Br2+2H2O=4H++SO42-+2Br-、![]() ;(2)由从海带中提取碘的实验分析可得结论,故答案为:CEAD、分液漏斗、再打开分液漏斗活塞,使下层液体从下口放出,待下层液体刚好放出时,关闭分液漏斗活塞,再从上口将上层液体倒出;(3) 步骤①是为了将Fe2+氧化成Fe3+,并在控制合适的pH条件时生成Fe(OH)3沉淀而除之,虽然漂液和H2O2都可采用,但对比表2提供的原料价格可以看出,漂液比H2O2的价格低得多,所以选漂液最合理,故X为漂液;加入Y的目的是使镁离子沉淀,Y为纯碱,故答案为:ClO-+2H++2Fe2+=2Fe3++Cl-+H2O、 MgCO3+H2OMg(OH)2+CO2↑。
;(2)由从海带中提取碘的实验分析可得结论,故答案为:CEAD、分液漏斗、再打开分液漏斗活塞,使下层液体从下口放出,待下层液体刚好放出时,关闭分液漏斗活塞,再从上口将上层液体倒出;(3) 步骤①是为了将Fe2+氧化成Fe3+,并在控制合适的pH条件时生成Fe(OH)3沉淀而除之,虽然漂液和H2O2都可采用,但对比表2提供的原料价格可以看出,漂液比H2O2的价格低得多,所以选漂液最合理,故X为漂液;加入Y的目的是使镁离子沉淀,Y为纯碱,故答案为:ClO-+2H++2Fe2+=2Fe3++Cl-+H2O、 MgCO3+H2OMg(OH)2+CO2↑。

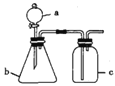
【题目】装置a、b、c中分别盛有试剂1、2、3,用如图所示的装置进行实验(夹持仪器略去,必要时可加热),能达到相应实验目的的是
选项 | 试剂1 | 试剂2 | 试剂3 | 实验目的 | 装置 |
A | 浓 | Cu片 | KI-淀粉溶液 | 验证 |
|
B | 盐酸 | 石灰石 | 饱和 | 制备 | |
C | 稀硫酸 | 溶液X | 澄清石灰水 | 验证溶液X中是否有 | |
D | 70%硫酸 |
| 酸性 | 证明 |
A. A B. B C. C D. D