题目内容
4.工业上用洗净的废铜屑作原料来制备硝酸铜,为了节约原料,宜采取的方法是( )| A. | Cu+HNO3(浓)→Cu(NO3)2 | |
| B. | Cu+HNO3(稀)→Cu(NO3)2 | |
| C. | Cu$→_{△}^{空气}$Cu$\stackrel{HNO_{3}}{→}$Cu(NO3)2 | |
| D. | Cu $→_{△}^{浓硫酸}$ CuSO4$\stackrel{Ba(NO_{3})_{2}}{→}$Cu(NO3)2 |
分析 为了节约原料,则反应中消耗的原料少,但该反应中不生成有毒气体,以此来解答.
解答 解:A.Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,二氧化氮有毒而污染环境,所以不符合条件,故A不选;
B.3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,NO有毒会污染环境,所以不符合条件,故B不选;
C.2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO、CuO+2HNO3=Cu(NO3)2+H2O,该反应中没有有毒气体生成,且能节约硝酸,所以符合条件,故C选;
D.Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O、CuSO4+Ba(NO3)2=BaSO4↓+Cu(NO3)2,该过程中生成有毒气体二氧化硫且浪费浓硫酸、硝酸钡,所以不符合条件,故D不选;
故选C.
点评 本题考查化学实验方案评价,为高频考点,明确反应条件、反应物的量、反应生成物的性质即可解答,要注意结合节约、环保理念分析解答,正确书写方程式是解本题关键,题目难度不大.

练习册系列答案
相关题目
15.下列有关化学用语表示不正确的是( )
| A. | 甲酸乙酯的结构简式:HCOOCH2CH3 | |
| B. | 质子数为53,中子数为75的碘原子:${\;}_{53}^{128}$I | |
| C. | 四氯化碳的电子式: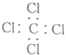 | |
| D. | 间甲基苯酚: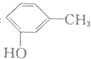 |
12.当光束通过肥皂水溶液时,从侧面观察到一条明亮的“光道”,说明肥皂水溶液属于( )
| A. | 溶液 | B. | 胶体 | C. | 悬浊液 | D. | 乳浊液 |
19.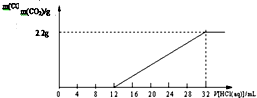 某碳酸钾和碳酸氢钾的混合样品61.4g,加水溶解后,取所得溶液的$\frac{1}{10}$,向其中缓缓加入一定浓度的稀盐酸,并同时记录放出CO2的质量和消耗稀盐酸的体积,得到如图所示的曲线,下列说法不正确的是( )
某碳酸钾和碳酸氢钾的混合样品61.4g,加水溶解后,取所得溶液的$\frac{1}{10}$,向其中缓缓加入一定浓度的稀盐酸,并同时记录放出CO2的质量和消耗稀盐酸的体积,得到如图所示的曲线,下列说法不正确的是( )
 某碳酸钾和碳酸氢钾的混合样品61.4g,加水溶解后,取所得溶液的$\frac{1}{10}$,向其中缓缓加入一定浓度的稀盐酸,并同时记录放出CO2的质量和消耗稀盐酸的体积,得到如图所示的曲线,下列说法不正确的是( )
某碳酸钾和碳酸氢钾的混合样品61.4g,加水溶解后,取所得溶液的$\frac{1}{10}$,向其中缓缓加入一定浓度的稀盐酸,并同时记录放出CO2的质量和消耗稀盐酸的体积,得到如图所示的曲线,下列说法不正确的是( )| A. | 该过程所发生反应的化学方程式:K2CO3+HCl═KCl+KHNO3,KHNO3+HCl═KCl+H2O+CO2↑ | |
| B. | 混合样品中碳元素的质量分数为8.5% | |
| C. | 混合样品中含碳酸钾41.4g | |
| D. | 将原混合液体充分加热后,再加入足量的盐酸,整个过程中产生的CO2总量不变 |
13.海带中含丰富的碘元素,从海带中分离出碘可按如下步骤进行:①滴加稀硫酸酸化后,加入适量H2O2(质量分数为3%) ②将海带焙烧成灰后加水搅拌 ③加CCl4振荡 ④用分液漏斗分液 ⑤煮沸、过滤.合理的操作顺序是( )
| A. | ①②③④⑤ | B. | ①③⑤②④ | C. | ②⑤①③④ | D. | ②①③⑤④ |
14. 短周期元素W、X、Y、Z在元素周期表中的位置如图所示,下列说法正确的( )
短周期元素W、X、Y、Z在元素周期表中的位置如图所示,下列说法正确的( )
 短周期元素W、X、Y、Z在元素周期表中的位置如图所示,下列说法正确的( )
短周期元素W、X、Y、Z在元素周期表中的位置如图所示,下列说法正确的( )| A. | W的非金属元素比Z的弱 | |
| B. | W的最高价氧化物对应的水化物是强酸 | |
| C. | Y的原子半径在同周期主族元素中最大 | |
| D. | Z的气态氢化物的稳定性在同主族元素中最强 |