题目内容
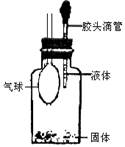
如图是实验室制备SO2并验证SO2某些性质的装置图。试回答:
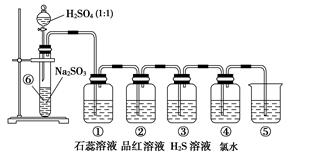
(1)⑥中发生的化学反应方程式为______________________________________(2分)
(2)⑤的作用是_______________________________________________________(2分),
反应的离子方程式为___________________________________________________(2分)
(3)填表格(每空1分)

(1)⑥中发生的化学反应方程式为______________________________________(2分)
(2)⑤的作用是_______________________________________________________(2分),
反应的离子方程式为___________________________________________________(2分)
(3)填表格(每空1分)
| 装置 | 实验现象 | 体现SO2的性质 |
| ① | | |
| ② | | |
| ③ | | |
| ④ | | |
(1)Na2SO3+H2SO4===Na2SO4+H2O+SO2↑(2分)
(2)吸收过量的SO2,防止污染环境 SO2+2OH-===SO+H2O(2分)
(3)( 每空1分)
(2)吸收过量的SO2,防止污染环境 SO2+2OH-===SO+H2O(2分)
(3)( 每空1分)
| 装置 | 实验现象 | 体现SO2的性质 |
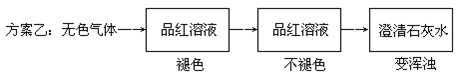
| ① | 溶液变红色 | SO2水溶液显酸性 |
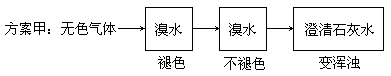
| ② | 溶液退色 | 漂白性 |
| ③ | 溶液变浑浊 | 氧化性 |
| ④ | 氯水退色 | 还原性 |
试题分析:(1)硫酸和亚硫酸钠反应生成SO2,则⑥中发生的化学反应方程式为Na2SO3+H2SO4=Na2SO4+H2O+SO2↑。
(2)SO2是大气污染物,因此氢氧化钠溶液的作用是吸收过量的SO2,防止污染环境,反应的离子方程式为SO2+2OH-=SO+H2O。
(3)SO2是酸性氧化物,溶于水显酸性,石蕊试液变红色;SO2具有漂泊性,能使品红溶液褪色;SO2具有氧化性,能把H2S氧化生成单质S沉淀;另外SO2还具有还原性,能被氯水氧化,使氯水褪色。2的制备、SO2性质的检验以及尾气处理
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重对学生实验能力的培养和解题方法的指导,有助于培养学生规范、严谨的实验设计和评价能力。该类试题主要是以实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确性及灵活运用知识解决实际问题的能力。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目