题目内容
【题目】某种钠空气水电池的充、放电过程原理示意图如图所示,下列有关说法错误的是
■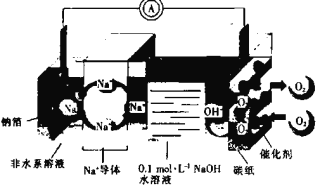
A.放电时,Na+向正极移动
B.放电时,电子由钠箔经过导线流向碳纸
C.充电时,当有0.1mole-通过导线时,则钠箔增重2.3g
D.充电时,碳纸与电源负极相连,电极反应式为4OH--4e=2H2O+O2↑
【答案】D
【解析】
A.放电时,电解质溶液中阳离子朝正极迁移,阴离子朝负极迁移,故Na+朝正极移动,A项正确;
B.电池放电时,钠箔做负极,碳纸为正极,电子在外电路中迁移方向是从负极流向正极,B项正确;
C.充电时,钠箔发生的电极反应为:![]() ,所以若有0.1mol e-通过导线,钠箔处就会析出0.1mol的钠单质,质量增加2.3g,C项正确;
,所以若有0.1mol e-通过导线,钠箔处就会析出0.1mol的钠单质,质量增加2.3g,C项正确;
D.碳纸在电池放电时做正极,所以充电时应与电源的正极相连,电极连接错误;但此选项中电极反应式书写是正确的,D项错误;
答案选D。

 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案【题目】(1)①为了纪念元素周期表诞生150周年,联合国将2019年定为“国际化学元素周期表年”。Fe在元素周期表中的位置为__________。科学家在研究金属矿物质组分的过程中。发现了Cu-Ni-Fe等多种金属互化物。确定某种金属互化物是晶体还是非晶体的方法是_____________。
②已知:r(Fe2+)为61 pm,r(Co2+)为65 pm。在隔绝空气条件下分别加热FeCO3和CoCO3,实验测得FeCO3的分解温度低于CoCO3,原因是_______。
③下表是Fe和Cu的部分电离能数据,请解释I2(Cu)大于I2(Fe)的主要原因是_____。
元素 | Fe | Cu |
第一电离能I1/kJ·mol-1 | 759 | 746 |
第一电离能I2/kJ·mol-1 | 1561 | 1958 |
(2)原子序数依次增大的五种元素A、B、C、D、E分别处于第一至第四周期,A是前四周期中原子半径最小的元素,B原子核外电子有6种不同的运动状态,常温下C的单质是空气中含量最多的成份,D最高价氧化物对应水化物的酸性最强,E的基态原子的最外能层只有一个电子,其他能层均已充满电子。请回答下列问题:
①B2A2的电子式是___,D所在主族的前四种元素分别与A形成的化合物,其共价键的极性由强到弱的顺序是___(填化学式)。
②A和C形成的简单化合物遇到D单质出现白烟现象,写出有关反应的化学方程式为____。
③向E的硫酸盐溶液中滴加过量氨水,观察到的现象是首先形成蓝色沉淀,继续滴加氨水,沉淀溶解,得到深蓝色的透明溶液,请写出最后-步得到深蓝色透明溶液对应的离子方程式____。
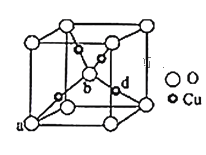
(3)铜与氧元素可形成如图所示的晶胞结构,其中Cu均匀地分散在立方体内部,a、b的坐标参数依次为(0,0,0)、(![]() ,
,![]() ,
,![]() ),则d的坐标参数为__,已知该品体的密度为ρg/cm3,NA是阿伏加德罗常数值,则晶胞参数(晶胞棱长)为_______cm(列出计算式即可)。
),则d的坐标参数为__,已知该品体的密度为ρg/cm3,NA是阿伏加德罗常数值,则晶胞参数(晶胞棱长)为_______cm(列出计算式即可)。