题目内容
3.铁是一种应用广泛的金属.下列有关铁的说法错误的是( )| A. | 铁在氧气中燃烧生成四氧化三铁 | B. | 常温下,铁在浓硫酸中会发生钝化 | ||
| C. | 铁与盐酸反应生成氯化铁与氢气 | D. | 铁是一种银白色金属 |
分析 A.铁在氧气中燃烧生成黑色的四氧化三铁;
B.常温下,铁和浓硫酸反应生成一层致密的氧化物薄膜;
C.铁和盐酸反应生成氯化亚铁和氢气;
D.铁是一种银白色金属单质.
解答 解:A.氧气氧化性较强,能将铁氧化为黑色的四氧化三铁,四氧化三铁又称磁性铁,故A正确;
B.常温下,铁和浓硫酸反应生成一层致密的氧化物薄膜而阻止进一步被氧化,该现象是钝化现象,所以常温下可以用铁制容器运输浓硫酸,故B正确;
C.盐酸氧化性较弱,铁和盐酸反应生成氯化亚铁和氢气,铁在氯气中燃烧生成氯化铁,故C错误;
D.纯铁为银白色金属,为金属的通性,故D正确;
故选C.
点评 本题考查铁的性质,涉及铁与氧气、浓硫酸、盐酸的反应,注意铁是变价金属,和强氧化剂反应生成高价铁,和弱氧化剂生成低价铁,题目难度不大.

练习册系列答案
相关题目
13.下列化学用语中,正确的是( )
| A. | 用电子式表示溴化氢的形成过程为: | |
| B. | 海水中Br-的电子式为: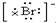 | |
| C. | 海水中通入氯气时发生反应的离子方程式为:2NaBr+Cl2=Br2+2NaCl | |
| D. | 氯离子的结构示意图为: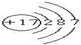 |
14.下列有关金属腐蚀与防护的说法不正确的是( )
| A. | 钢铁在弱碱性条件下发生电化学腐蚀的正极反应是:O2+2H2O+4e-═4OH- | |
| B. | 可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 | |
| C. | 在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 | |
| D. | 当镀锌铁制品的镀层破损时,镀层仍能对铁制品起保护作用 |
11.下列物质既能与KMnO4酸性溶液反应,又能与溴水反应的一组物质是( )
①苯 ②苯酚 ③甲苯 ④乙醇 ⑤己烯 ⑥己烷 ⑦亚硫酸.
①苯 ②苯酚 ③甲苯 ④乙醇 ⑤己烯 ⑥己烷 ⑦亚硫酸.
| A. | ②③⑤⑥ | B. | ②④⑥⑦ | C. | ②⑤⑦ | D. | 全部 |
18.下列说法不正确的是( )
| A. | 同族元素,随着电子层的增加,I1逐渐增大 | |
| B. | 通常情况下,电离能I1<I2<I3 | |
| C. | 同周期元素,随着核电荷数的增加,I1呈增大趋势 | |
| D. | 电离能越小,元素的金属性越强 |
8.下列排列顺序正确的是( )
| A. | 微粒半径:Na+>K+>Cl->S2- | B. | 稳定性:HI>HBr>HCl>HF | ||
| C. | 酸性:HClO4>H2SO4>H3PO4>H2SiO4 | D. | 熔点:Al>Mg>Na>K |
15.用含有A12O3、SiO2和少量FeO•xFe2O3的铝灰来制备A12(SO4)3.18H2O.,工艺流程如下(部分操作和条件略):
Ⅰ、向铝灰中加入过量稀H2SO4,过滤:
Ⅱ、向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ、加热,产生大量棕色沉淀,静置,上层溶液呈紫红色:
Ⅳ、加入MnSO4至紫红色消失,过滤;
Ⅴ、浓缩、结晶、分离,得到产品.
(1)铝在元素周期表中的位置第三周期ⅢA族;H2SO4溶解Al2O3的离子方程式是:Al2O3+6H+=2Al3++3H2O.
(2)写出Ⅱ中加入过量KMnO4溶液发生的离子方程式:5Fe2++8H++MnO4-=Mn2++5Fe3++4H2O.
(3)已知:生成氢氧化物沉淀的pH
注:金属离子的起始浓度为0.1mol•L-1
根据表中数据解释步骤Ⅱ的目的:将Fe2+氧化为Fe3+,调节pH值使铁元素完全沉淀.
(4)己知:一定条件下,MnO4-可与Mn2+反应生成MnO2.
①向Ⅲ的沉淀中加入浓HCI并加热,能说明沉淀中存在MnO2的现象是生成黄绿色气体.
②Ⅳ中加入MnSO4的目的是除去过量的MnO4-.
(5)在该实验条件下Ksp[Fe(OH)3]=4.0×10-38,当溶液的pH=3时,溶液中c(Fe3+)=4.0×10-5 mol/L.
Ⅰ、向铝灰中加入过量稀H2SO4,过滤:
Ⅱ、向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ、加热,产生大量棕色沉淀,静置,上层溶液呈紫红色:
Ⅳ、加入MnSO4至紫红色消失,过滤;
Ⅴ、浓缩、结晶、分离,得到产品.
(1)铝在元素周期表中的位置第三周期ⅢA族;H2SO4溶解Al2O3的离子方程式是:Al2O3+6H+=2Al3++3H2O.
(2)写出Ⅱ中加入过量KMnO4溶液发生的离子方程式:5Fe2++8H++MnO4-=Mn2++5Fe3++4H2O.
(3)已知:生成氢氧化物沉淀的pH
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
根据表中数据解释步骤Ⅱ的目的:将Fe2+氧化为Fe3+,调节pH值使铁元素完全沉淀.
(4)己知:一定条件下,MnO4-可与Mn2+反应生成MnO2.
①向Ⅲ的沉淀中加入浓HCI并加热,能说明沉淀中存在MnO2的现象是生成黄绿色气体.
②Ⅳ中加入MnSO4的目的是除去过量的MnO4-.
(5)在该实验条件下Ksp[Fe(OH)3]=4.0×10-38,当溶液的pH=3时,溶液中c(Fe3+)=4.0×10-5 mol/L.
12.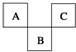 如图是周期表中短周期的一部分,A、B、C三种元素原子核外电子数之和等于B的质量数.B原子核内质子数和中子数相等.下面叙述中不正确的是( )
如图是周期表中短周期的一部分,A、B、C三种元素原子核外电子数之和等于B的质量数.B原子核内质子数和中子数相等.下面叙述中不正确的是( )
 如图是周期表中短周期的一部分,A、B、C三种元素原子核外电子数之和等于B的质量数.B原子核内质子数和中子数相等.下面叙述中不正确的是( )
如图是周期表中短周期的一部分,A、B、C三种元素原子核外电子数之和等于B的质量数.B原子核内质子数和中子数相等.下面叙述中不正确的是( )| A. | 三种元素的原子半径的大小顺序是B<A<C | |
| B. | A元素最高价氧化物对应水化物具有强氧化性和不稳定性 | |
| C. | B元素的氧化物和氢化物的水溶液都呈酸性 | |
| D. | C元素的单质是非金属单质中唯一能跟水激烈反应的单质 |
13.某短周期非金属元素的原子核外最外层电子数是次外层电子数的一半,该元素( )
| A. | 单质常用作半导体材料和光导纤 | B. | 在自然界中以化合态的形式存在 | ||
| C. | 最高价氧化物不与任何酸反应 | D. | 气态氢化物比甲烷稳定 |