题目内容
【题目】碳元素及其化合物与人类的生活、生产息息相关,请回答下列问题:
(1)自然界中的碳循环对人类的生存与发展具有重要意义。
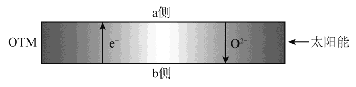
①绿色植物的光合作用吸收CO2释放O2的过程可以描述为以下两步:
2CO2(g)+2H2O(l)+2C5H10O4(s) = 4(C3H6O3)+(s)+O2(g)+4e- △H=+1360 kJ·mol-1
12(C3H6O3)+(s)+12e- = C6H12O6(s,葡萄糖)+6C5H10O4(s)+3O2(g) △H=-1200 kJ·mol-1
则绿色植物利用二氧化碳和水合成葡萄糖并放出氧气的热化学方程式为:_________________。
②溶洞的形成是石灰岩中的主要成分碳酸钙在一定条件下溶解和沉积形成,请站在活化能的角度解释溶洞形成过程极为缓慢的原因____________。
(2) 工业上碳及其化合物是重要的工业原料。
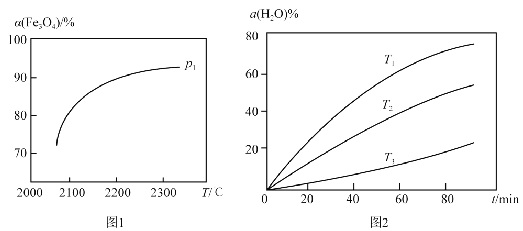
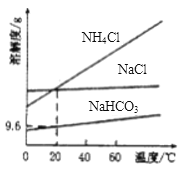
①以CO2、NaCl、NH3为原料制得Na2CO3是“侯氏制碱法”的重要步骤,相关物质的溶解度曲线如图所示,请写出常温下向饱和氯化钠溶液中先后通入足量的NH3、CO2发生反应的离子方程式:___。
常温常压下,在NaHCO3溶液中存在如下平衡:
HCO3-+H2O![]() H2CO3+OH- Kh=2.27×10-8
H2CO3+OH- Kh=2.27×10-8
HCO3- ![]() CO32-+H+ Ka2=4.7×10-11
CO32-+H+ Ka2=4.7×10-11
H2O![]() H++OH- Kw=1.0×10-14
H++OH- Kw=1.0×10-14
请用K定量解释NaHCO3溶液显碱性的原因:____________,在NaHCO3溶液中继续通入CO2,至溶液中n(HCO3-):n(H2CO3)= ____________时溶液可以达中性。
②工业上可以利用甲醇制备氢气。
甲醇蒸汽重整法制备氢气的胡政尧反应为CH3OH(g) ![]() CO(g)+2H2(g),设在容积为2.0L的密闭容器中充入0.60mol的CH3OH(g)体系压强为p1,在一定条件下达到平衡时,体系压强为p2,且p2:p1=2.2,则该条件下CH3OH的平衡转化率为__________________。
CO(g)+2H2(g),设在容积为2.0L的密闭容器中充入0.60mol的CH3OH(g)体系压强为p1,在一定条件下达到平衡时,体系压强为p2,且p2:p1=2.2,则该条件下CH3OH的平衡转化率为__________________。
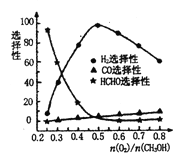
工业上还可以利用甲醇部分氧化法制备氢气,在一定温度下以Ag/CeO2-ZnO为催化剂,原料气比例对反应选择性(选择性越大,表示生成的该物质越多)影响关系如图所示.则当
n(O2)/n(CH3OH)=0.25时,CH3OH与O2发生的主要反应方程式为__________;在制备H2时最好控制n(O2)/n(CH3OH)=________。
【答案】 6CO2(g)+6H2O(1)=C6H12O6(s,葡萄糖)+6O2(g) ΔH=+2880KJ/mol 溶洞形成过程的化学反应在自然条件下活化能较高 NH3+CO2+H2O+Na+=Na2HCO3↓+NH4+或NH3+CO2+H2O=NH4++HCO3-、NH4++HCO3-+Na+=NaHCO3↓+NH4+ Na2HCO3溶液中的水解平衡常数大于HCO3-的电离常数 4.4 60% 2CH3OH+O2![]() 2HCHO+2H2O 0.5
2HCHO+2H2O 0.5
【解析】(1)①已知热化学方程式:2CO2(g)+2H2O(l)+2C5H10O4(s)═4(C3H6O3)+(s)+O2(g)+4e-△H═+1360kJmol-1 ①;12(C3H6O3)+(s)+12e-= C6H12O6(s,葡萄糖)+6C5H10O4(s)+3O2(g) △H=-1200 kJ·mol-1②;根据盖斯定律,将①×3+②可得:6CO2(g)+6H2O(l)=C6H12O6(s)+6O2(g)△H=+2880kJmol-1;
②溶洞的形成是石灰岩中的主要成分碳酸钙在一定条件下溶解和沉积形成,但 溶洞形成过程的化学反应在自然条件下活化能较高,则形成过程极为缓慢;
(2) ①根据溶解度曲线可知常温下NaHCO3的溶解度明显小于NaCl,向饱和氯化钠溶液中先后通入足量的NH3、CO2将有NaHCO3析出,发生反应的离子方程式NH3+CO2+H2O+Na+=Na2HCO3↓+NH4+。
因Na2HCO3溶液中的水解平衡常数大于HCO3-的电离常数,故NaHCO3溶液显碱性;溶液为中性,则c(H+)=10-7mol/L,K=![]() =4.4×10-7,则溶液中n(HCO3-):n(H2CO3)=
=4.4×10-7,则溶液中n(HCO3-):n(H2CO3)=![]() =4.4;
=4.4;
② CH3OH(g)![]() CO(g)+2H2(g)
CO(g)+2H2(g)
起始量/mol 0.60 0 0
转化量/mol xx 2x
平衡量/mol0.60-x x 2x
气体压强之比等于气体物质的量之比, ![]() =2.2,解得x=0.36;CH3OH的转化率=
=2.2,解得x=0.36;CH3OH的转化率=![]() ×100%=60%;当n(O2)/n(CH3OH)=0.25时,CH3OH与O2发生的主要反应为甲醇的催化氧化生成甲醛,反应的方程式为:2CH3OH+O2
×100%=60%;当n(O2)/n(CH3OH)=0.25时,CH3OH与O2发生的主要反应为甲醇的催化氧化生成甲醛,反应的方程式为:2CH3OH+O2![]() 2HCHO+2H2O;依据图象分析,在制备H2时最好控制n(O2)/n(CH3OH)=0.5时氢气生成最多。
2HCHO+2H2O;依据图象分析,在制备H2时最好控制n(O2)/n(CH3OH)=0.5时氢气生成最多。