题目内容
【题目】将32.5gZn投入到vmL浓硫酸中,共热,恰好完全反应,则可以确定的数据是( )
A.所得气体在标准状况下的体积 B.所得气体的质量
C.所得溶液的浓度 D.原硫酸的浓度
【答案】A
【解析】
试题分析:32.5g锌是0.5mol,与浓硫酸反应生成硫酸锌、SO2和H2O,随着反应的进行,浓硫酸的浓度逐渐减小,稀硫酸与锌反应生成硫酸锌和氢气,且总是1mol锌产生1mol氢气、1molSO2,所以可以计算产生的气体在标准状况下的体积。由于不能确定氢气和SO2的体积之比,所以不能计算氢气和SO2的物质的量,以及消耗的硫酸的物质的量,反应后溶液的体积不能确定,则不能计算反应后溶液的浓度,答案选A。

 世纪百通期末金卷系列答案
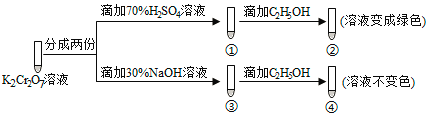
世纪百通期末金卷系列答案【题目】某地环保部门取一定量某工厂所排废水试样分成甲、乙、丙、丁四份,进行如图所示探究。
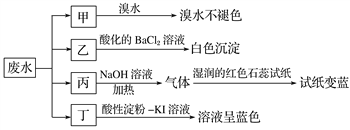
已知废水试样中可能含有下表中的离子:
离子 | |
阳离子 | Na+、Mg2+、X |
阴离子 | Cl-、SO |
请回答下列问题:
(1)离子X是______________(填化学式,下同),离子Y是__________________。
(2)表中不能确定是否存在的阴离子是__________。
(3)写出废水试样中滴加酸性淀粉KI溶液所发生反应的离子方程式: ___________________。
【题目】参考下列(a)~(c)项回答问题:
(a)皂化值是使1g油脂皂化所需要的KOH的毫克数。
(b)碘值是使100g油脂加成碘的克数。
(c)各种油脂的皂化值、碘值列表如下:
花生油 | 亚麻仁油 | 牛油 | 黄油 | 硬化大豆油 | 大豆油 | |
皂化值 | 190 | 180 | 195 | 226 | 193 | 193 |
碘值 | 90 | 182 | 38 | 38 | 5 | 126 |
(1)单纯由(C17H33COO)3C3H5(相对分子质量884)形成的油,皂化值是
(2)在横线上填入适当的词句:
亚麻仁油比花生油所含的_________________多,黄油比牛油的_________________小。硬化大
豆油的碘值小的原因是_________ ________。
(3)为使碘值为180的鱼油100 g硬化所需要的H2的体积为 升(标准状况下)?
(4)结构简式为 的酯,若皂化值为430,求n为
的酯,若皂化值为430,求n为