题目内容
11.高温下,在容积固定的密闭容器中,用足量焦炭与一定量二氧化碳发生可逆的吸热反应生成了CO.达到化学平衡之后,保持其他条件不变,移走少量CO,达到新的平衡时,下列选项中,增大的是 ( )a、CO2和CO浓度比 b、混合气体的密度
c、转化率 d、CO的体积分数.
分析 高温下,在容积固定的密闭容器中,用足量焦炭与一定量二氧化碳发生可逆的吸热反应生成了CO,反应的化学方程式为:C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO,反应达到平衡状态后移走少量CO,平衡正向进行,结合反应特征和平衡移动原理分析判断选项.
解答 解:C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO,反应达到平衡状态后移走少量CO,平衡正向进行,
a、平衡正向进行,二氧化碳减小,一氧化碳增加,CO2和CO浓度比减小,故a不符合;
b、移走少量CO,平衡正向进行,气体质量减小,体积不变,混合气体的密度减小,故b不符合;
c、移走少量CO,平衡正向进行反应物转化率增大,故c符合;
d、移走少量CO,达到新的平衡时二氧化碳减小,一氧化碳增多,所以CO的体积分数增大,故d符合;
故选:cd.
点评 本题考查了化学平衡影响因素分析判断,主要是改变物质浓度对反应平衡的理解应用,注意一氧化碳体积分数的变化分析,掌握基础是解题关键,题目难度中等.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案
相关题目
1.电解CuSO4和NaCl的混合溶液,开始阴极和阳极上分别析出的物质是( )
| A. | H2和Cl2 | B. | Cu和Cl2 | C. | H2和O2 | D. | Cu和O2 |
2.等物质的量浓度的下列稀溶液:①CH3COONa溶液;②Na2CO3溶液;③X溶液;④Ba(OH)2溶液.它们的pH依次增大,则X溶液不可能是( )
| A. | 氨水 | B. | 硅酸钠溶液 | C. | NaOH溶液 | D. | NaHCO3溶液 |
19.下表列出了前20号元素中的某些元素性质的有关数据:
试回答下列问题:
(1)以上10种元素的原子中,最容易失去电子的是②(填写编号);与H2最容易化合的非金属单质是氟气(写物质名称).
(2)写出元素⑤的氢化物结构式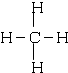 ;③和⑤形成的化合物的电子式
;③和⑤形成的化合物的电子式 ;写出元素③和⑧形成的既有离子键,又有共价键的化合物的电子式
;写出元素③和⑧形成的既有离子键,又有共价键的化合物的电子式 ;
;
(3)某元素R的原子半径为1.02×10-10m,该元素在周期表中的位置第三周期第VIA族.
(4)写出上述⑥、⑦两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的一种物质的分子式PCl3.
(5)试比较⑤和⑨两元素的最高价氧化物对应的水化物的酸性强弱(填化学式):HClO4>HNO3
(6)写出④的最高价氧化物分别跟⑦和⑧的最高价氧化物的水化物反应的离子方程式OH-+Al(OH)3=AlO2-+2H2O,Al(OH)3+3H+=Al3++3H2O.
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
| 原子半径 (10-10m) | 1.52 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 0.71 |
| 最高价态 | +1 | +1 | -- | +3 | +4 | +5 | +7 | +1 | +5 | -- |
| 最低价态 | -- | -- | -2 | -- | -4 | -3 | -1 | -- | -3 | -1 |
(1)以上10种元素的原子中,最容易失去电子的是②(填写编号);与H2最容易化合的非金属单质是氟气(写物质名称).
(2)写出元素⑤的氢化物结构式
 ;③和⑤形成的化合物的电子式
;③和⑤形成的化合物的电子式 ;写出元素③和⑧形成的既有离子键,又有共价键的化合物的电子式
;写出元素③和⑧形成的既有离子键,又有共价键的化合物的电子式 ;
;(3)某元素R的原子半径为1.02×10-10m,该元素在周期表中的位置第三周期第VIA族.
(4)写出上述⑥、⑦两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的一种物质的分子式PCl3.
(5)试比较⑤和⑨两元素的最高价氧化物对应的水化物的酸性强弱(填化学式):HClO4>HNO3
(6)写出④的最高价氧化物分别跟⑦和⑧的最高价氧化物的水化物反应的离子方程式OH-+Al(OH)3=AlO2-+2H2O,Al(OH)3+3H+=Al3++3H2O.
6.下列关于苯的说法中,正确的是( )
| A. | 试管中加入少量苯,加入溴水振荡后,溴水褪色,发生了加成反应 | |
| B. | 苯能使酸性高锰酸钾溶液褪色 | |
| C. | 苯较难发生加成反应,所以通常要加入催化剂 | |
| D. | 苯不能发生取代反应 |
16.下列说法中正确的是( )
| A. | 球棍模型 表示的有机物是乙烯 表示的有机物是乙烯 | |
| B. | 电子式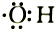 可以表示羟基,也可以表示氢氧根 可以表示羟基,也可以表示氢氧根 | |
| C. | 有机物 的分子式为C6H8O2 的分子式为C6H8O2 | |
| D. | 结构简式(CH3)2CHOH:可以表示1-丙醇,也可以表示2-丙醇 |
3.分子式为C6H12O2且与NaHCO3反应放出CO2的有机化合物有(不考虑立体结构)( )
| A. | 8种 | B. | 7种 | C. | 6种 | D. | 5种 |
20.已知,金刚石的燃烧热为395kJ/mol,下表是部分化学键的键能数据,下列选项中正确的是:
| 化学键 | C-C | O=O | C=O |
| 键能(kJ/mol) | 348 | 498 | x |
| A. | X=794.5 | |
| B. | X=1142.5 | |
| C. | 1mol金刚石的能量一定比1molCO2能量高 | |
| D. | 金刚石燃烧的热化学方程式为2C(s)+O2(g)=2CO(g)△H=790kJ/mol |