题目内容
【题目】按要求完成下列空白:
(1)9gNH4+的物质的量为___,其中含电子的数目为___。(用NA表示)
(2)同温同压下:同体积的氨气和甲烷气体的质量比为___,同质量的氨气和甲烷气体的体积比为___。
(3)已知24克A和40克B恰好完全反应生成0.4molC和32克D,则C的摩尔质量为___。
(4)某无土栽培营养液中含有NH4+、Cl-、 K+、 SO42-,测得含0.6mol/LNH4+、0.5mol/LCl-、0.5mol/LK+,则SO42-的物质的量浓度为___。
【答案】0.5mol 5NA(或3.01×1024) 17:16 16:17 80g/mol 0.3mol/L
【解析】
(1)9gNH4+的物质的量为![]() 0.5mol,1个NH4+含有10个电子,其中含电子的数目为0.5mol×10 ×NA=5NA。
0.5mol,1个NH4+含有10个电子,其中含电子的数目为0.5mol×10 ×NA=5NA。
(2)根据阿伏伽德罗定律,同温同压下:同体积的氨气和甲烷气体的物质的量相等,设物质的量均为nmol,质量比为(nmol×17g/mol): (nmol×16g/mol)= 17:16,同质量的氨气和甲烷气体,设质量为mg,则物质的量分别是![]() 、
、![]() ,根据阿伏伽德罗定律,同温同压下,气体的体积比等于物质的量比,所以体积比为
,根据阿伏伽德罗定律,同温同压下,气体的体积比等于物质的量比,所以体积比为![]() :
:![]() =16:17。
=16:17。
(3)24克A和40克B恰好完全反应生成0.4molC和32克D,根据质量守恒,生成C的质量是24g+40g-32g=32g,则C的摩尔质量为![]() g/mol。
g/mol。
(4)某营养液中含有NH4+、Cl-、 K+、 SO42-,根据电荷守恒, 0.6mol/L ×1+0.5mol/L×1=0.5mol/L×1+2c(SO42-),c(SO42-)= 0.3mol/L。

 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案【题目】H2是一种重要的清洁能源。
(1)已知:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH2=-49.0kJmol-1
CH3OH(g)+H2O(g) ΔH2=-49.0kJmol-1
CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH3=-41.1kJmol-1
CO2(g)+H2(g) ΔH3=-41.1kJmol-1
H2还原 CO反应合成甲醇的热化学方程式为:CO(g)+2H2(g)![]() CH3OH(g) ΔH1,则ΔH1=___kJmol-1,该反应自发进行的条件为___
CH3OH(g) ΔH1,则ΔH1=___kJmol-1,该反应自发进行的条件为___
A.高温 B.低温 C.任何温度条件下
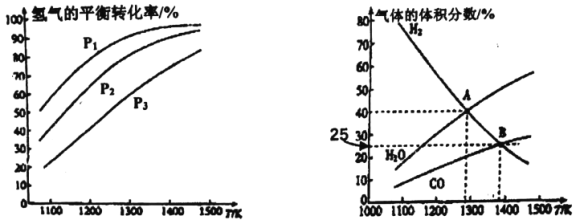
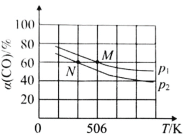
(2)恒温恒压下,在容积可变的密闭容器中加入 1molCO和2.2mol H2,发生反应CO(g)+2H2(g)![]() CH3OH(g),实验测得平衡时CO的转化率随温度、压强的变化如图所示。则P1__P2,判断的理由是_____。
CH3OH(g),实验测得平衡时CO的转化率随温度、压强的变化如图所示。则P1__P2,判断的理由是_____。
(3)若反应 CO(g)+2H2(g)![]() CH3OH(g)在温度不变且体积恒定为1的密闭容器中发生,反应过程中各物质的物质的量随时间变化如表所示:
CH3OH(g)在温度不变且体积恒定为1的密闭容器中发生,反应过程中各物质的物质的量随时间变化如表所示:
时间/min | 0 | 5 | 10 | 15 |
H2 | 4 | 2 | ||
CO | 2 | 1 | ||
CH3OH(g) | 0 | 0.7 |
①下列各项能作为判断该反应达到平衡标志的是____(填字母);
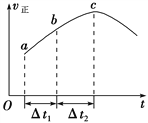
A.容器内压强保持不变 B.2v正
C.混合气体的相对分子质量保持不变 D.混合气体的密度保持不变
②若起始压强为P0 kPa,则在该温度下反应的平衡常数Kp=___(kPa)-2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
③反应速率若用单位时间内分压的变化表示,则10min内H2的反应速率v(H2)=___kPamin-1。