题目内容
【题目】某课外活动小组进行Fe(OH)3胶体的制备实验并检验其性质。
(1)现有甲、乙两名同学进行制备实验:
①甲同学的操作是:取一小烧杯,加入25ml蒸馏水加热至沸腾,向沸水中逐滴加入1~2mlFeCl3饱和溶液,继续煮沸至混合液呈红褐色,停止加热。请评价该操作是否正确__________。(填“正确”或“不正确”,下同)
②乙向沸水中滴加饱和FeCl3溶液,为了使反应充分进行,煮沸10分钟,请评价是否正确__________。
(2)写出制备Fe(OH)3胶体的化学方程式:_________________________________。
(3)聪明的你还想出来许多在家里观察丁达尔效应的方法,请设计一个你认为最简单、最环保的办法:________________________________________________。
【答案】正确 不正确 FeCl3+3H2O![]() Fe(OH)3(胶体)+3HCl 打开装有热水的暖瓶盖,用一束光照射升腾的水汽即可
Fe(OH)3(胶体)+3HCl 打开装有热水的暖瓶盖,用一束光照射升腾的水汽即可
【解析】
(1)①制取氢氧化铁胶体的方法是:取一小烧杯,加入25ml蒸馏水加热至沸腾,向沸水中逐滴加入1~2mlFeCl3饱和溶液,继续煮沸至混合液呈红褐色,停止加热。故①甲正确。
②乙向沸水中滴加饱和FeCl3溶液,为了使反应充分进行,煮沸10分钟使胶体发生聚沉,所以此法不正确;
(2)向沸水中逐滴加入1~2mlFeCl3饱和溶液,继续煮沸至混合液呈红褐色,停止加热,制得Fe(OH)3胶体的化学方程式:FeCl3+3H2O![]() Fe(OH)3(胶体)+3HCl
Fe(OH)3(胶体)+3HCl
(3)打开装有热水的暖瓶盖,用一束光照射升腾的水汽即可。

 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案【题目】探究电场作用下阴阳离子的迁移。a、b、c、d 均为石墨电极,电极间距4cm。将pH试纸用不同浓度Na2SO4溶液充分润湿,进行如下实验:
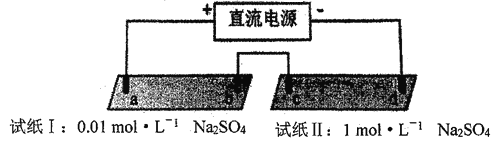
实验现象:
时间 | 试纸I | 试纸II |
lmin | a极附近试纸变红,b极附近试纸变蓝 | c极附近试纸变红,d极附近…… |
10min | 红色区和蓝色区不断向中间扩展,相遇时红色区约2.7cm,蓝色区约1.3cm | 两极颜色范围扩大不明显,试纸大部分仍为黄色 |
下列说法不正确的是
A. d极附近试纸变蓝
B. a极附近试纸变红的原因是:2H2O+2e-= H2↑+2OH-
C. 对比试纸I和试纸II的现象,说明电解质浓度环境影响H+和OH-的迁移
D. 试纸I的现象说明,此环境中H+的迁移速率比OH-快