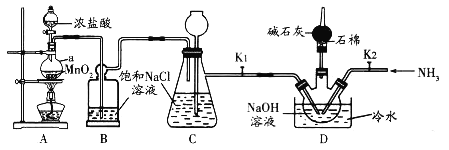
题目内容
【题目】某溶液中可能含有Na+、Al3+、Fe2+、Fe3+、Cu2+、Ag+、CO32-、S2-、SO32-、AlO2-、Cl-、SO42-中的一种或几种,对该溶液进行实验,结果如图:

下列说法不正确的是( )
A. 淡黄色沉淀甲为AgBr,沉淀乙为Al(OH)3
B. 溶液中一定含有Na+、S2-、SO32-、AlO2-
C. 气体甲的成分可能是CO2或SO2或H2S或CO2、SO2的混合气体或CO2、H2S的混合气体
D. 确定溶液A中是否含有SO42-,可在沉淀丙中加入足量稀盐酸,若沉淀部分溶解则溶液A中含有SO42-,若沉淀全部溶解则溶液A中不含SO42-
【答案】A
【解析】
与过量的溴化氢反应生成气体甲和淡黄色沉淀,沉淀若是溴化银,则不存在题中所给的各种阴离子,所以淡黄色沉淀为单质硫,HBr与S2-、SO32-反应生成S单质和SO2或H2S气体,而S2-、SO32-与Al3+、Fe2+、Fe3+、Cu2+结合生成沉淀或发生双水解而不共存,即溶液中一定含S2-、SO32-,一定不含Al3+、Fe2+、Fe3+、Cu2+,根据电荷守恒,一定含有Na+,溶液甲中含有过量的溴化氢,与过量的碳酸氢铵反应,生成的气体乙为二氧化碳,白色沉淀只能为氢氧化铝,说明原溶液中一定含有AlO2-,溶液乙与过量的氢氧化钡溶液反应,生成的气体为氨气,白色沉淀为碳酸钡或硫酸钡,但白色沉淀丙与CO2能反应,故丙为碳酸钡,即原溶液中不含SO42-,又因为加入的NH4HCO3能引入HCO3-,故不能确定原溶液中是否含有CO32-。所以原溶液中一定存在的离子有:Na+、S2-、SO32-、AlO2-,一定不存在的离子有Al3+、Fe2+、Fe3+、Cu2+、Ag+、SO42-,可能存在的离子有CO32-、Cl-。
A.因为Ag+不能存在,故沉淀甲不可能为AgBr,故A错误;
B.根据上述分析,原溶液中一定含有Na+、S2-、SO32-、AlO2-,故B正确;
C.因溶液中一定含有S2-、SO32-,可能含有CO32-,在与过量的HBr反应时生成的气体可能为CO2或SO2或H2S或CO2和SO2的混合气体或CO2和H2S的混合气体,故C正确;
D.BaSO4是不溶于稀盐酸的沉淀,BaCO3是可溶于稀盐酸的沉淀,向沉淀丙中加入足量稀盐酸,若沉淀部分溶解则溶液A中含有SO42-,若沉淀全部溶解则溶液A中不含SO42-,故D正确。答案选A。