题目内容
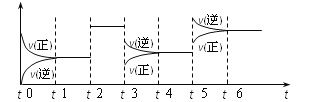
【题目】某密闭容器中发生如下反应:X(g)+3Y(g)![]() 2Z(g);ΔH<0。下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是( )
2Z(g);ΔH<0。下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是( )
A. t5时增大了压强 B. t3时降低了温度
C. t2时加入了催化剂 D. t4~t5时间内转化率一定最低
【答案】C
【解析】
三步分析法:一看反应速率是增大还是减小;二看Δv正、Δv逆的相对大小;三看化学平衡移动的方向。由图可知:t2~t3时,Δv正=Δv逆>0, 化学平衡不移动,t2时加入了催化剂;t3~t4时,v(逆)、v(正)均减小,且Δv正>Δv逆,化学平衡逆移,t3时是减小压强;t5~t6时,v(逆)、v(正)均增大,且Δv逆>Δv正,化学平衡逆移,t5时是升高温度;由化学平衡移动原理可知:t6时X的转化率最低。所以本题答案为C。

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目
【题目】下列实验操作规范且能达到目的的是
目的 | 操作 | |
A. | 取20.00 mL盐酸 | 在50 mL酸式滴定管中装入盐酸,调整初始读数为30.00 mL后,将剩余盐酸放入锥形瓶 |
B. | 测定醋酸钠溶液pH | 用玻璃棒蘸取溶液,点在湿润的pH试纸上 |
C. | 清洗碘升华实验所用试管 | 先用酒精清洗,再用水清洗 |
D. | 配制浓度为0.010 | 称取KMnO4固体0.158 g,放入100 mL容量瓶中,加水溶解并稀释至刻度 |
A. A B. B C. C D. D