��Ŀ����
����Ŀ�������仯������NH3����Ρ�N2H4��N2O4������ѧ��ѧ��������ҵ������������ռ����Ҫ��λ��
��1�����亽����������(N2H4)��N2O4��ȼ������ȼ������(N2H4)��N2O4�ķ�ӦΪ2N2H4(1)+N2O4(g)=3N2(g)+4H2O(g) ��H = -1077 kJ/mol
��֪��ط�Ӧ�Ļ�ѧ�������������£�
![]()
��ʹ1 mol N2O4(g)�����л�ѧ����ȫ����ʱ��Ҫ���յ�������__________ ��
��2��N2O4��NO2֮����ڷ�ӦN2O4(g)![]() 2NO2(g)����һ������N2O4��������ܱ������У������ƽ��ת����[��(N2O4)]���¶ȵı仯��ͼ��ʾ��
2NO2(g)����һ������N2O4��������ܱ������У������ƽ��ת����[��(N2O4)]���¶ȵı仯��ͼ��ʾ��
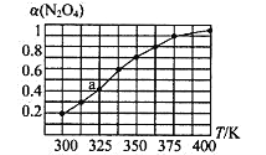
����ͼ�Ʋ�÷�Ӧ��H_______0���>����<����������Ϊ______________ ��
��ͼ��a���Ӧ�¶��£���֪N2O4����ʼѹǿp0Ϊ108 kPa������¶��·�Ӧ��ƽ�ⳣ��Ϊ��Kp=_____________����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�����ʵ�������,ȡ��λ��Ч���֣���
����һ�������£��÷�ӦN2O4��NO2����������������ѹǿ����ڹ�ϵ��v(N2O4)=k1p(N2O4)��v(NO2)=k2p2(NO2)������k1��k2���뷴Ӧ�¶��йصij�������Ӧ�����ʣ�ѹǿ��ϵ��ͼ��ʾ��һ���¶��£�k1��k2��ƽ�ⳣ��Kp�Ĺ�ϵ��k1=________������ͼ����ĵ��У��ܱ�ʾ��Ӧ�ﵽƽ��״̬�ĵ�Ϊ______��

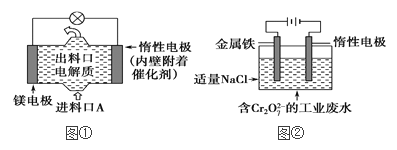
��3�����NO2�Ʊ�NH4NO3���乤��ԭ����ͼ��ʾ��
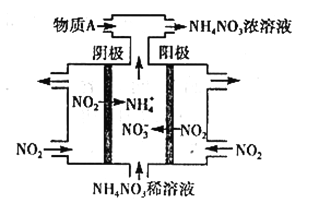
�������ĵ缫��ӦʽΪ_______________________��
��Ϊʹ������ȫ��ת��ΪNH4NO3���貹������A����A�Ļ�ѧʽΪ___________��
���𰸡� 1941 kJ > �¶����ߣ�����N2O4�����ӣ�˵��ƽ�����ơ��÷�ӦΪ���ȷ�Ӧ����H>0 115.2KPa ![]() B����D�� NO2-e-+H2O=NO3-+2H+ NH3
B����D�� NO2-e-+H2O=NO3-+2H+ NH3
����������1�����ݷ�Ӧ���ʱ��H=��Ӧ���ܼ���-�������ܼ��ܼ��㣻
��2���ٸ����¶ȶ�ƽ��״̬��Ӱ����ͼ������ж��ʱ䣻
�ڸ��ݷ�Ӧ����ʽ����ƽ��ʱ��ϵ��N2O4��NO2�ķ�ѹ�����뻯ѧƽ�ⳣ������ʽ�����ѹƽ�ⳣ����
�۵��ﵽ��ѧƽ��ʱ����v��=v�����ݴ����㻯ѧƽ�ⳣ������ʽ��������������2v��N2O4��=v��NO2���жϻ�ѧƽ��ĵ㣻
��3���ٵ�����������������Ӧ������ԭ��ͼ������NO2������ʧȥ����ת��ΪNO3-���ݴ�д�������ĵ缫��Ӧʽ��
�ڸ��ݷ�Ӧʽ�ж�A���ʡ�
��1����H=8E��N-H��+2E��N-N��+E��N2O4��-3E��N��N��-8��O-H��=-1077kJ/mol�����������ݴ��뼴�ɽ��E��N2O4��=1941kJ/mol����ʹ1 mol N2O4(g)�����л�ѧ����ȫ����ʱ��Ҫ���յ�������1941kJ��
��2���ٸ���ͼ������������¶����ߣ�N2O4��ƽ��ת��������˵�������¶������ڷ�Ӧ������У������ʱ��H��0��
��N2O4��NO2֮����ڷ�ӦN2O4(g)![]() 2NO2(g)��a����ʼʱN2O4��ѹǿΪ108kPa��N2O4��ƽ��ת����Ϊ40%����
2NO2(g)��a����ʼʱN2O4��ѹǿΪ108kPa��N2O4��ƽ��ת����Ϊ40%����
N2O4(g)![]() 2NO2(g)
2NO2(g)
��ʼ����mol�� 1 0
ת������mol�� 0.4 0.8
ƽ������mol�� 0.6 0.8
��ƽ��ʱѹǿΪ1.4p0
���Է�Ӧ�ķ�ѹƽ�ⳣ��ΪKp=p2(NO2)/p(N2O4)= ��
��
�۵��ﵽ��ѧƽ��ʱ����v��=v��������������2v��N2O4��=v��NO2��������v��N2O4��=k1p��N2O4����v��NO2��=k2p2��NO2������k1��k2��ƽ�ⳣ��Kp�Ĺ�ϵΪk1=![]() ������2v��N2O4��=v��NO2��������Ա�ʾ��ѧƽ��ĵ�ΪB���D�㣻
������2v��N2O4��=v��NO2��������Ա�ʾ��ѧƽ��ĵ�ΪB���D�㣻
��3���ٵ�����������������Ӧ������ԭ��ͼ������NO2������ʧȥ����ת��ΪNO3-���������ĵ缫��ӦʽΪ��NO2-e-+H2O=NO3-+2H+��
��������ӦʽΪNO2+7e-+8H+��NH4++2H2O�����������H+��ΪʹNO2���ȫ��ת��ΪNH4NO3������Ҫ��Ӧ��H+����NH4+�����Լ����A����ӦΪNH3��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ��ijѧϰС��ͨ������װ��̽�� MnO2��FeCl3��6H2O�ܷ�Ӧ����Cl2��
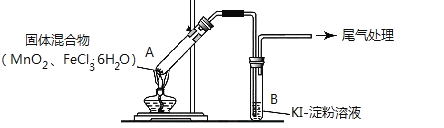
ʵ��������������±���
ʵ���� | ���� | ���� |
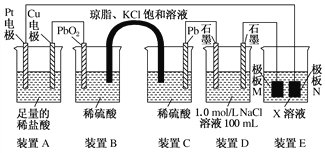
ʵ�� 1 | ����ͼ��ʾ����MnO2��FeCl3��6H2O����� | ���Թ�A�в��ֹ����ܽ⣬�Ϸ����ְ��� ���Ժ�����ɫ���壬�ܱڸ��Ż�ɫҺ�� ���Թ�B����Һ���� |
ʵ�� 2 | ��A�еĻ���ﻻΪFeCl3��6H2O��B����Һ��ΪKSCN��Һ�����ȡ� | A�в��ֹ����ܽ⣬���������ͻ�ɫ���壬B��KSCN��Һ��� |
�ش��������⣺
��1��ʵ��1��ʵ��2����������ԭ����___________________________��
��2��ʵ��2˵����ɫ�����к���___________���ѧʽ����ʵ��1�Т۵�����Ҳ�����Ƿ�������һ�����ӷ�Ӧ,�������ӷ���ʽΪ______________________________��
��3��Ϊ��һ��ȷ�ϻ�ɫ�����к���Cl2����ѧϰС���ʵ��1������ָĽ�������
����1����A��B ������ʢ��ij���Լ���ϴ��ƿC�����B����Һ�Ա�Ϊ��ɫ��
����2����B�е���KI��Һ�滻ΪNaBr��Һ�����B����Һ�ʳȺ�ɫ����δ���Fe2+��
��1��C��ʢ�ŵ��Լ���_________________������2�м��� Fe2+���Լ�������____________��ѡ��NaBr��Һ��������__________________��
��4��ʵ��1��ּ��Ⱥ�����Ӧ�б�������δ����������Ԫ������֮��Ϊ1:2����A�з�����Ӧ�Ļ�ѧ����ʽΪ____________________________��
��5����ѧϰС����Ϊʵ��1����Һ���������ܻ�������һ��ԭ����__________���������ʵ�鷽����֤�˲���__________________________��