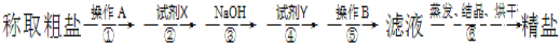题目内容
【题目】铋酸钠( NaBiO3 )是一种难溶于水的强氧化剂,在钢铁工业中常用作锰元素的分析测定。某研究小组用浮选过的辉铋矿(主要成分是Bi2S3,还含少量Bi2O3,SiO2等杂质)制备铋酸钠,其流程如下:

请回答下列问题:
(1)为了提高“浸取”中原料的浸出率,可以采取的措施是_________________(写一种即可) 。
(2)“浸取”时通常加入FeCl3溶液和浓盐酸,向其中加入过量浓盐酸的目的是_____,“滤渣”的成份是____________(填化学式)。
(3)“沉淀”反应的离子方程式为__________________________________________________;
(4)“沉淀”操作时,用氨水调节pH至6,通过计算说明,此时溶液中的Bi3+是否完全沉淀:____________________(已知:Bi(OH)3的溶度积Ksp=3×10-32) 。
(5)“焙烧”除了采用最佳的质量比、合适的温度外,你认为还需要控制的条件是________。
(6)已知,在酸性溶液中NaBiO3将Mn2+氧化为MnO4-。请出该反应的离子方程式:__________。
(7)某辉铋矿中铋元素的质量分数为20.90%,若100吨该辉铋矿完全用于生产,共得到25.00吨NaBiO3,则产率是___________。
【答案】将矿石粉碎(或适当提高温度或增大FeCl3溶液的浓度) 防止FeCl3及BiCl3水解生成不溶性沉淀,提高原料的浸出率 SiO2 S Bi3+ + 3NH3H2O==Bi(OH)3↓+3NH4+ 当pH=6时,溶液中c(OH-)=1×10-8 molL-1此时溶液中c(Bi3+)=Ksp[Bi(OH)3]/c3(OH-)=3×10-32/(1×10-8)3=3×10-8 molL-1 由于溶液中c(Bi3+)<1×10-5 molL-1,说明Bi3+已经完全沉淀 控制干燥且无CO2的环境 5NaBiO3+2Mn2++14H+==2MnO4-+5Na++5Bi3++7H2O 89.29%
【解析】
(1)提高浸取率的措施可以是将矿石粉碎(或适当提高温度或增大FeCl3溶液的浓度)等;
(2)“浸取”时通常加入FeCl3溶液和浓盐酸,向其中加入过量浓盐酸的目的是防止FeCl3及BiCl3水解生成不溶性沉淀,提高原料的浸出率,二氧化硅不溶于盐酸,且铁离子将硫离子氧化产生的硫单质不溶于酸,故“滤渣”的成份是SiO2 、S;
(3)“沉淀”反应是利用氨水将Bi3+转化为沉淀,同时生成铵盐,反应的离子方程式为Bi3+ + 3NH3H2O==Bi(OH)3↓+3NH4+;
(4)“沉淀”操作时,用氨水调节pH至6,c(OH-)=10-8mol/L,c(Bi3+)=![]() =
=![]() =3×10-8 mol/L <10-5 mol/L,此时溶液中的Bi3+已完全沉淀;
=3×10-8 mol/L <10-5 mol/L,此时溶液中的Bi3+已完全沉淀;
(5)“焙烧”除了采用最佳的质量比、合适的温度外,还需要控制控制干燥且无CO2的环境;
(6)已知,在酸性溶液中NaBiO3将Mn2+氧化为MnO4-,本身被还原为Bi3+,转移电子数为10电子 ,根据氧化还原反应原理配平得,反应的离子方程式为:5NaBiO3+2Mn2++14H+==2MnO4-+5Na++5Bi3++7H2O;
(7)某辉铋矿中铋元素的质量分数为20.90%,若100吨该辉铋矿完全用于生产,共得到25.00吨NaBiO3,则产率是![]() 。
。