题目内容
下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
(1)④、⑤、⑥的原子半径由大到小的顺序是
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式: 或
或 
 或
或  .
.
(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(5)写出⑥的最高价氧化物对应水化物的电离方程式
| 族 周期 |
ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
Na>Al>O
Na>Al>O
.(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
HNO3>H2CO3>H2SiO3
HNO3>H2CO3>H2SiO3
.(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:
 或
或 
 或
或 
(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为
ab
ab
(填序号).a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(5)写出⑥的最高价氧化物对应水化物的电离方程式
AlO2-+H++H2O?Al(OH)3?Al3++3OH-
AlO2-+H++H2O?Al(OH)3?Al3++3OH-
.分析:根据元素在周期表中的分布,可以知道①是H,②是C,③是N,④是O,⑤是Na,⑥是Al,⑦是Si,⑧是Cl,
(1)同周期自左而右原子半径减小,同主族自上而下原子半径增大,据此判断;
(2)非金属性越强,最高价氧化物对应水化物的酸性越强;
(3))①、④、⑤、⑧中的某些元素形成的NaOH、NaClO等既含离子键又含极性共价键;
(4)两种元素的原子按1:1组成的常见液态化合物为H2O2;
(5)氢氧化铝是两性氢氧化物,存在酸式电离与碱式电离.
(1)同周期自左而右原子半径减小,同主族自上而下原子半径增大,据此判断;
(2)非金属性越强,最高价氧化物对应水化物的酸性越强;
(3))①、④、⑤、⑧中的某些元素形成的NaOH、NaClO等既含离子键又含极性共价键;
(4)两种元素的原子按1:1组成的常见液态化合物为H2O2;
(5)氢氧化铝是两性氢氧化物,存在酸式电离与碱式电离.
解答:解:根据元素在周期表中的分布,可以知道①是H,②是C,③是N,④是O,⑤是Na,⑥是Al,⑦是Si,⑧是Cl,
(1)同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径Na>Al>O,
故答案为:Na>Al>O;
(2)②、③、⑦对应的元素分别为C、N、Si,非金属性:N>C>Si,元素的非金属性越强,对应的最高价含氧酸的酸性越强,则HNO3>H2CO3>H2SiO3 ,
故答案为:HNO3>H2CO3>H2SiO3 ;
(3)①、④、⑤、⑧中的某些元素形成NaOH、NaClO等既含离子键又含极性共价键,电子式分别为 、
、 ,
,
故答案为: 或
或  ;
;
(4)两种元素的原子按1:1组成的常见液态化合物为H2O2,在MnO2或FeCl3催化作用下分解,而Na2SO3具有还原性,与H2O2发生氧化还原反应,不能用作催化剂,高锰酸钾具有强氧化性,与H2O2发生氧化还原反应,也不能作催化剂,
故答案为:ab;
(5)氢氧化铝是两性氢氧化物,存在酸式电离与碱式电离,电离方程式为:AlO2-+H++H2O?Al(OH)3?Al3++3OH-,
故答案为:AlO2-+H++H2O?Al(OH)3?Al3++3OH-.
(1)同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径Na>Al>O,
故答案为:Na>Al>O;
(2)②、③、⑦对应的元素分别为C、N、Si,非金属性:N>C>Si,元素的非金属性越强,对应的最高价含氧酸的酸性越强,则HNO3>H2CO3>H2SiO3 ,
故答案为:HNO3>H2CO3>H2SiO3 ;
(3)①、④、⑤、⑧中的某些元素形成NaOH、NaClO等既含离子键又含极性共价键,电子式分别为
 、
、 ,
,故答案为:
 或
或  ;
;(4)两种元素的原子按1:1组成的常见液态化合物为H2O2,在MnO2或FeCl3催化作用下分解,而Na2SO3具有还原性,与H2O2发生氧化还原反应,不能用作催化剂,高锰酸钾具有强氧化性,与H2O2发生氧化还原反应,也不能作催化剂,
故答案为:ab;
(5)氢氧化铝是两性氢氧化物,存在酸式电离与碱式电离,电离方程式为:AlO2-+H++H2O?Al(OH)3?Al3++3OH-,
故答案为:AlO2-+H++H2O?Al(OH)3?Al3++3OH-.
点评:本题考查元素的推断,题目难度中等,根据元素在周期表中的物质可推断出元素的种类,题中侧重于周期律的应用,学习中注意积累相关知识,注意把握电子式的书写.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目








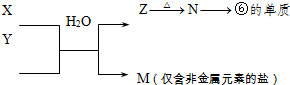
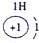
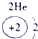
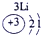
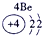
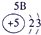
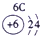
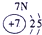
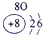
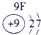
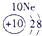
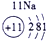





 表示的是
表示的是