题目内容
在火箭推进器中装有还原剂液态肼(N2H4)和强氧化剂液态H2O2,当它们混合时,即产生大量的氮气和水蒸气,并放出大量的热量。已知一些键断裂所需能量数据:
N-N:159 kJ /mol N="N:419" kJ /mol N≡N:945 kJ /mol H-H:436 kJ /mol
N-H:389 kJ /mol H-O:465 kJ /mol O-O:138 kJ /mol O="O:498" kJ /mol
①写出肼和过氧化氢的结构式:肼______ ___,过氧化氢______
②写出肼和双氧水反应的热化学方程式_____________________________。
N-N:159 kJ /mol N="N:419" kJ /mol N≡N:945 kJ /mol H-H:436 kJ /mol
N-H:389 kJ /mol H-O:465 kJ /mol O-O:138 kJ /mol O="O:498" kJ /mol
①写出肼和过氧化氢的结构式:肼______ ___,过氧化氢______
②写出肼和双氧水反应的热化学方程式_____________________________。
①
②N2H4(l) + 2H2O2(l) = N2(g)+4H2O(g);△H=" —814" KJ/mol

②N2H4(l) + 2H2O2(l) = N2(g)+4H2O(g);△H=" —814" KJ/mol
①根据肼和双氧水的结构简式可知,二者的结构式是 。
。
②反应热就是断键吸收的热量和形成化学键所放出的能量的差值,所以该反应的反应热是4×389 kJ /mol+159 kJ /mol+2×2×465 kJ /mol+2×138 kJ /mol-4×2×465 kJ /mol-945 kJ /mol =—814 KJ/mol,所以该反应的热化学方程式是N2H4(l) + 2H2O2(l) = N2(g)+4H2O(g);△H=" —814" KJ/mol。
 。
。②反应热就是断键吸收的热量和形成化学键所放出的能量的差值,所以该反应的反应热是4×389 kJ /mol+159 kJ /mol+2×2×465 kJ /mol+2×138 kJ /mol-4×2×465 kJ /mol-945 kJ /mol =—814 KJ/mol,所以该反应的热化学方程式是N2H4(l) + 2H2O2(l) = N2(g)+4H2O(g);△H=" —814" KJ/mol。

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
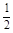 O2(g) =H2O(l) △H2=–285.8 kJ/mol
O2(g) =H2O(l) △H2=–285.8 kJ/mol
 (aq)+Ba2+(aq)+2OH-(aq)===BaSO4(s)+2H2O(l) △H=-114.6 kJ·mol-1
(aq)+Ba2+(aq)+2OH-(aq)===BaSO4(s)+2H2O(l) △H=-114.6 kJ·mol-1 2NH3(g)△H="—38.6" kJ·mol—1
2NH3(g)△H="—38.6" kJ·mol—1