题目内容
X、Y、Z和W代表原子序数依次增大的四种短周期元素,X原子核内没有中子,在元素周期表中,Z与Y、W均相邻;Y、Z和W三种元素的原子最外层电子数之和为17。则下列有关叙述正确的是( )
| A.Y、Z和W三种元素可能位于同一周期 |
| B.上述元素形成的氢化物中,W的氢化物相对分子质量最大,熔、沸点最高 |
| C.Y和W所形成的含氧酸均为强酸 |
| D.X、Y、Z和W可以组成原子的物质的量之比为5∶1∶4∶1的离子化合物 |
D
解析试题分析:原子核内没有中子的原子为H,如果Y、Z和W为同周期相邻,则最外层电子数可分别认为是n-1、n、n+1,之和为3n,是3的倍数,现在17不是3的倍数,所以不是同周期相邻,一般是两个同周期,两个同主族,所以最外层电子分别为n-1、n、n,之和为3n-1,或是n、n、n+1,之和为3n+1,也就是就这个和与3的倍数差1,这个倍数就是其中两种元素的主族数.该题中17=18-1,18为6的倍数,所以有两种元素位于第6主族,短周期中只有O和S,O的原子序数为8,S的原子序数为16,则另一种原子的原子序数为31-8-16=7,为N元素,所以X为H元素,Y、Z和W应分别是N、O、S元素。A选项,Y、Z和W三种元素的原子最外层电子数之和为17,不是3的倍数,所以不是同周期相邻,故A错误;B选项,因H2O或H2O2的熔沸点均比H2S高,故B错误;C选项,亚硝酸、亚硫酸虽然属于含氧酸,但都是弱酸,故C错误;D选项,离子化合物NH4HSO4中氢、氮、氧、硫的原子个数比为5:1:4:1,即H5NO4S,故D正确。
考点:原子结构与元素周期率的关系

元素周期表中铋元素的数据见图,下列说法正确的是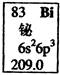
| A.Bi元素的质量数是209 |
| B.Bi元素的相对原子质量是209.0 |
| C.Bi原子6p亚层有一个未成对电子 |
| D.Bi原子最外层有5个能量相同的电子 |
下列说法正确的是( )
| A.常温常压下,只有一种元素的单质呈液态 |
| B.元素周期表中所有元素都是从自然界中发现的 |
| C.过渡元素不全是金属元素 |
| D.常温常压下,气态单质的分子都是由非金属元素的原子形成的 |
短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外层电子数之比为4︰3, Z原子比X原子的核外电子数多4。下列说法正确的是 ( )
| A.W、Y、Z的氢化物稳定性顺序可能是W>Z>Y |
| B.W、X、Y、Z的原子半径大小顺序Z<Y<X<W |
| C.Z的氧化物对应水化物的酸性一定强于W氧化物对应水化物的酸性 |
| D.Z的某种氧化物可以做新型消毒剂 |
下列说法正确的是
| A.元素铯的两种核素137Cs比133Cs多四个质子 |
| B.等质量的H2、D2、T2三种气体的电子数之比为2∶3∶6 |
| C.一种元素只能有一种质量数 |
| D.在氮原子中,质子数为7而中子数不一定为7 |
现有某氯化钠(Na37Cl)6克,其中含钠元素的质量为( )
| A.2克 | B.2.3克 | C.3克 | D.都不对 |
元素的性质呈周期性变化的根本原因是 ( )
| A.元素原子量的递增,量变引起质变 |
| B.元素的原子半径呈周期性变化 |
| C.元素的金属性和非金属性呈周期性变化 |
| D.元素原子的核外电子排布呈周期变化 |
下列叙述中正确的是
| A.两种微粒,若核外电子排布完全相同,其化学性质也一定相同 |
| B.凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布 |
| C.两种原子若核外电子排布相同,则一定属于同种元素 |
| D.存在两种质子数和电子数均相同的阳离子和阴离子 |