题目内容
【题目】某有机物A是农药生产中的一种中间体,其结构简式如图所示,下列叙述正确的是( )
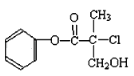
A. 有机物A属于芳香烃
B. 有机物A可以和Br2的CCl4溶液发生加成反应
C. 有机物A和浓硫酸混合加热,可以发生消去反应
D. 1molA和足量的NaOH溶液反应,可以消耗3mol NaOH
【答案】D
【解析】试题A.该物质中除了含有C、H元素外,还含有O元素,不属于芳香烃,A项错误;B.该分子中没有碳碳不饱和键,不能与溴发生加成反应,B项错误;C.醇分子中,连有羟基(-OH)的碳原子必须有相邻的碳原子且此相邻的碳原子上有氢原子时,才可发生消去反应,即该化合物分子中的羟基不能发生消去反应,氯原子可以发生消去反应,但是需要在NaOH的醇溶液中加热,C项错误;D.由于酯基水解后又生成1个酚羟基,所以1molA和足量的NaOH溶液反应,最多可以消耗3molNaOH,D项正确;答案选D。

 金钥匙试卷系列答案
金钥匙试卷系列答案【题目】现有部分短周期元素的性质或原子结构如下表:
元素编号 | 元素性质或原子结构 |
T | 单质能与水剧烈反应,所得溶液呈弱酸性 |
X | L层p电子数比s电子数多2个 |
Y | 第三周期元素的简单离子中半径最小 |
Z | L层有三个未成对电子 |
(1)写出元素X的离子结构示意图____________。
(2)写出Y元素最高价氧化物的水化物与NaOH溶液反应的离子方程式______________
(3)写出Y的价电子排布式_________________________。
(4)元素T与氯元素相比,非金属性较强的是_______(用元素符号表示),下列表述中能用于证明这一事实的是_______(填字母代号)。
A.气态氢化物的挥发性 B.两元素的电负性
C.含氧酸的酸性 D.氢化物中X—H键的键长(X代表T和Cl两种元素)
(5)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的单质中化学性质明显不同于其他三种单质的是___(填元素符号)
