题目内容
【题目】以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等.实验室模拟工业以硫酸渣制备铁红(Fe2O3),过程如图:
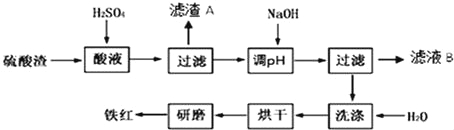
(1)硫酸渣的成分中既能与酸又能与碱反应的是 ,写出酸溶过程Fe2O3与稀硫酸反应的离子反应方程式: .
(2)生产过程中,为了确保铁红的纯度,氧化过程需要调节溶液的pH的范围是 (部分阳离子以氢氧化物形式沉淀时溶液的pH见表)
沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
开始沉淀 | 2.7 | 3.8 | 7.5 | 9.4 |
完全沉淀 | 3.2 | 5.2 | 9.7 | 12.4 |
(3)滤渣A的主要成分为 ,滤液B含有的主要物质有 .
(4)如何证明洗涤环节充分洗净 .
(5)已知硫酸渣质量为a kg,假设铁红制备过程中铁元素损耗25%,最终得到铁红的质量为b kg,则原来硫酸渣中铁元素质量分数为 .(用题中所给数据计算并用最简整数比表示结果)
【答案】(1)Al2O3;Fe2O3+6H+═2Fe3++3H2O;
(2)3.2﹣3.8;
(3)SiO2;Na2SO4、MgSO4、Al2(SO4)3;
(4)取少许最后一次洗涤滤液,滴入1~2滴Ba(NO3)2溶液,若不出现白色浑浊,表示已洗涤完全;
(5)![]() .
.
【解析】
试题分析:硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,稀硫酸溶解主要除去不与酸反应的SiO2,过滤得到滤渣A含有SiO2,滤液含有Fe3+、Al3+、Mg2+,再加氢氧化钠,调节溶液的pH的范围是3.2~3.8可得到Fe(OH)3,最后洗涤、烘干、研磨使氢氧化铁分解生成氧化铁,从而得到铁红,滤液B中含有Na2SO4、MgSO4、Al2(SO4)3,以此解答该题.
解:硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,稀硫酸溶解主要除去不与酸反应的SiO2,过滤得到滤渣A含有SiO2,滤液含有Fe3+、Al3+、Mg2+,再加氢氧化钠,调节溶液的pH的范围是3.2~3.8可得到Fe(OH)3,最后洗涤、烘干、研磨使氢氧化铁分解生成氧化铁,从而得到铁红,滤液B中含有Na2SO4、MgSO4、Al2(SO4)3,
(1)硫酸渣的成分中既能与酸又能与碱反应的是Al2O3,为两性氧化物,Fe2O3与稀硫酸反应的离子反应方程式为Fe2O3+6H+═2Fe3++3H2O,
故答案为:Al2O3;Fe2O3+6H+═2Fe3++3H2O;
(2)由表中数据可知调节溶液的pH的范围是3.2~3.8主要是使三价铁沉淀,而二价镁,三价铝都不沉淀,故答案为:3.2﹣3.8;
(3)由以上分析可知滤渣A的主要成分为SiO2,滤液B含有的主要物质有Na2SO4、MgSO4、Al2(SO4)3,
故答案为:SiO2;Na2SO4、MgSO4、Al2(SO4)3;
(4)固体具有吸附性,氢氧化铁固体表面吸附硫酸根离子,可取少许最后一次洗涤滤液,滴入1~2滴Ba(NO3)2溶液,若不出现白色浑浊,表示已洗涤完全,
故答案为:取少许最后一次洗涤滤液,滴入1~2滴Ba(NO3)2溶液,若不出现白色浑浊,表示已洗涤完全;
(5)铁红制备过程中铁元素的质量为(b×![]() )÷75%=
)÷75%=![]() ,则原来硫酸渣中铁元素质量分数为
,则原来硫酸渣中铁元素质量分数为![]() ,故答案为:
,故答案为:![]() .
.

 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案