题目内容
11.以下各分子中,所有原子都满足最外层8电子稳定结构的是( )| A. | NO2 | B. | BF3 | C. | PCl3 | D. | H3O+ |
分析 分子中原子的最外层电子数可以根据每种元素原子的最外层电子数与化合价的绝对值之和来判断.
解答 解:A、NO2,N原子最外层有5个电子,化合价为+4,5+4=9,不满足分子中所有原子都满足最外层8电子结构,故A正确;
B、BF3中,B元素位于第ⅢA族,则3+3≠8,不满足分子中所有原子都满足最外层8电子结构,故B错误;
C、PCl3中P元素化合价为+3,P原子最外层电子数为5,所以5+3=8,P原子满足8电子结构;Cl元素化合价为-1,Cl原子最外层电子数为7,所以1+7=8,Cl原子满足8电子结构,故C正确;
D、H3O+中含有氢原子,不满足8电子结构,故D错误.
故选C.
点评 本题考查原子的结构,本题中注意判断是否满足8电子结构的方法,注意利用化合价与最外层电子数来分析即可解答,明确所有原子都满足最外层8电子结构是解答的关键.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
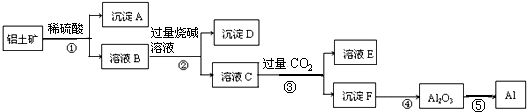
1.工业上以铝土矿(主要成分是Al2O3,含杂质Fe2O3和SiO2)为原料生产铝,其生产流程如下:
下列叙述错误的是( )

下列叙述错误的是( )
| A. | 沉淀A主要是SiO2 | B. | 步骤②的目的是分离Fe3+和Al3+ | ||
| C. | 溶液E溶质主要有碳酸钠和硫酸钠 | D. | ⑤主要是把电能转化为化学能 |
2.在标准状况下,进行甲、乙、丙三组实验:三组各取60mL同浓度盐酸,加入同一种镁铝合金粉末,产生气体,有关数据如表:
则下列说法正确的是( )
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 510 | 770 | 918 |
| 气体体积/mL | 560 | 672 | 672 |
| A. | 甲组和乙组的实验中,盐酸均是过量的 | |
| B. | 盐酸的物质的量浓度为0.8 mol/L | |
| C. | 合金中镁铝的物质的量之比为1:1 | |
| D. | 丙组中铝的物质的量为0.009 mol |
19.共价化合物含C、H、N三种元素.分子内有四个N原子,成四面体;每两个N原子之间都含有1个C原子.又知分子中无C一C键和C=C键,该化合物的分子式( )
| A. | C3H8N4 | B. | C6H12N4 | C. | C6H10N4 | D. | C4H8N4 |
6.下列化学措施不可行的是( )
| A. | 以 CH≡CH 和 HCl 反应制氯乙烯,进而制备聚氯乙烯塑料 | |
| B. | 浓氨水滴入生石灰中,将产生的气体通入 AlCl3溶液,可得到含AlO2-的溶液 | |
| C. | 使用催化剂不能改变工业合成 NH3 的反应限度 | |
| D. | 用浸有 KMnO4溶液的硅土来吸收水果释放的乙烯 |
16.元素电负性随原子序数的递增而增强的是( )
| A. | Na、K、Rb | B. | N、P、As | C. | Si、P、Cl | D. | O、S、Cl |
3.下列物质中,不能使溴水和高锰酸钾酸性溶液褪色的是( )
| A. | C2H4 | B. | C3H6 | C. | C2H2 | D. | C3H8 |
20.将10℃的饱和碳酸钠溶液升温至25℃,或者温度仍保持在10℃而加入少量无水碳酸钠,在这两种情况下均保持不变的是( )
| A. | 溶液中溶质的质量分数 | B. | 溶液中阳离子数目 | ||
| C. | 溶液的质量 | D. | 浓度 |
1.下列酸性氧化物和碱反应时,反应速率最慢的是( )
| A. | 二氧化碳气体通入氨水中 | B. | 二氧化硫气体通入澄清石灰水中 | ||
| C. | 五氧化二磷投入碱溶液中 | D. | 二氧化硅投入烧碱溶液中 |