题目内容
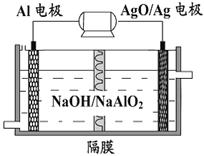
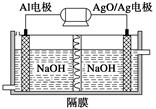
Al-AgO电池可用作水下动力电源,其原理如图所示。该电池反应的化学方程式为:
2Al+3 AgO+2NaOH=2NaAlO2+3Ag+H2O,则下列说法正确的是 ( )
2Al+3 AgO+2NaOH=2NaAlO2+3Ag+H2O,则下列说法正确的是 ( )

| A.当电极上析出0.54 g Ag时,电路中转移的电子为0.01 mol |
B.该隔膜是阳离子交换膜 |
| C.Al电极的反应式为:Al-3e-+3OH-=Al(OH)3 |
| D.正极的电极反应式为:AgO+2e-+2H+=Ag+H2O |
A
试题分析:该装置是原电池,结合电池反应铝失电子发生氧化反应作负极,电极反应为Al-3e-+4OH-=AlO2-+2H2O,AgO得电子发生还原反应为正极,正极上的电极反应式为AgO+2e-+H2O=Ag+2OH-,据此分析解答。A、根据正极上的电极反应式AgO+2e-+H2O=Ag+2OH-代入数据计算可得,正确;B、由两极的反应知该隔膜是阴离子交换膜,错误。

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目