题目内容
15.用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
①Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) △H= +64.39kJ·mol-1
②2H2O2(l)=2H2O (l)+O2(g) △H= -196.46kJ·mol-1
(l)+O2(g) △H= -196.46kJ·mol-1
③H2(g)+O2(g)=H2O(l) △H= -285.84kJ·mol-1
下列有关说法错误的是( )
①Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) △H= +64.39kJ·mol-1
②2H2O2(l)=2H2O
 (l)+O2(g) △H= -196.46kJ·mol-1
(l)+O2(g) △H= -196.46kJ·mol-1③H2(g)+O2(g)=H2O(l) △H= -285.84kJ·mol-1
下列有关说法错误的是( )
| A.铜可以溶解于稀盐酸与H2O2的混合溶液 |
| B.铜溶解于酸性双氧水的热化学方程式为: Cu(s)+H2O2(l)+2H+(aq)=Cu2+(aq)+2H2O(l) △H= —319.68 kJ·mol-  1 1 |
| C.反应①是在任何条件下都不可能发生的化学反应 |
| D.用H2O2和H2SO4的混合溶液溶解铜比用浓硫酸溶解铜环保 |
C
略

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
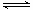 2NH3的能量变化如下图所示,该反应的热化学方程式是
2NH3的能量变化如下图所示,该反应的热化学方程式是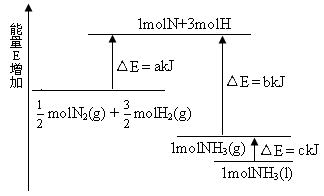
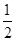 N2(g)+
N2(g)+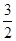 H2(g)
H2(g) 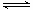 NH3(1) △H=(b+c-a)kJ·mol-1
NH3(1) △H=(b+c-a)kJ·mol-1 2SO3(g)
2SO3(g)  H = -190 kJ·mol-1
H = -190 kJ·mol-1 O2 (g) = CO2 (g)
O2 (g) = CO2 (g) 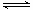 2SO3(g)反应过程的能量变化如图所示。请回答下列问题:
2SO3(g)反应过程的能量变化如图所示。请回答下列问题: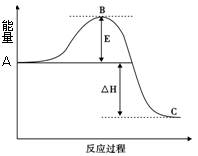
 ;如在相同温度下,在同等体积的密闭容器中充入2mol的SO3,也在V2O5催化剂存在时反应达到平衡,求此温度下反应2SO3 (g)
;如在相同温度下,在同等体积的密闭容器中充入2mol的SO3,也在V2O5催化剂存在时反应达到平衡,求此温度下反应2SO3 (g) 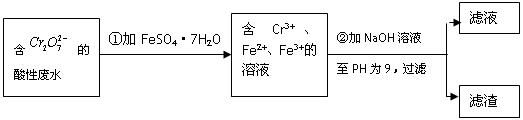
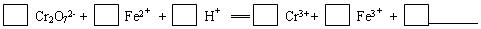
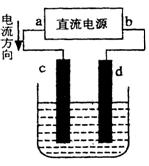
 CH3OH(g)进行过程中的能量变化曲线。曲线 a表示不使用催化剂时反应的能量变化,曲线 b表示使用催化剂后的能量变化。下列相关说法正确的是 ( )
CH3OH(g)进行过程中的能量变化曲线。曲线 a表示不使用催化剂时反应的能量变化,曲线 b表示使用催化剂后的能量变化。下列相关说法正确的是 ( )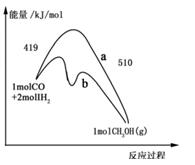

 ZnO(s);ΔH="-351.5" kJ·mol-1
ZnO(s);ΔH="-351.5" kJ·mol-1

 ,A的转化率
,A的转化率 与p、T的关系如图,根据图示可以得出的正确结论是
与p、T的关系如图,根据图示可以得出的正确结论是