题目内容
(Ⅰ)2SO2(g)+O2(g) 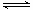 2SO3(g)反应过程的能量变化如图所示。请回答下列问题:
2SO3(g)反应过程的能量变化如图所示。请回答下列问题:
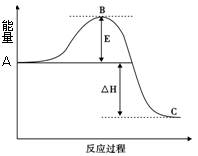
(1)图中A表示 。
(2)E的大小对该反应的焓变有无影响? 。
该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低? 。
(3)某温度下,向1L密闭容器中开始充入2molSO2和1molO2,在V2O5催化剂存在时反应达到平衡,压强减小为开始时的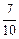 ;如在相同温度下,在同等体积的密闭容器中充入2mol的SO3,也在V2O5催化剂存在时反应达到平衡,求此温度下反应2SO3 (g)
;如在相同温度下,在同等体积的密闭容器中充入2mol的SO3,也在V2O5催化剂存在时反应达到平衡,求此温度下反应2SO3 (g) 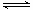 2SO2(g) + O2(g)的平衡常数(写出计算过程)
2SO2(g) + O2(g)的平衡常数(写出计算过程)
(Ⅱ)化学试剂的生产和电镀工业排放的废水中常含有20~100mg.L-1Cr(Ⅵ),饮用含Cr(Ⅵ)的水会损害人的肠胃等,已知Cr(Ⅲ)的毒性是Cr(Ⅵ)的0.5%,国家规定工业废水含Cr(Ⅵ)的量排放标准为0.1mg.L-1。工业上常用化学法和电解法处理含Cr(Ⅵ)废水,再将Cr(Ⅲ)转化成沉淀除去,某研究性学习小组为研究废水的净化,设计了如下实验流程:
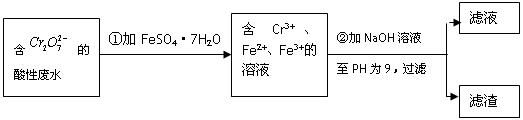
(1)配平第①步反应的离子方程式:
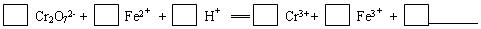
(2)第②步中用PH试纸测定溶液PH的操作是:
(3)设计一个电解装置也可以实现上述目的,装置如下图(用铁棒和石墨作电极):
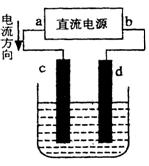
电极材料:c为:
电极反应:d极:
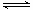 2SO3(g)反应过程的能量变化如图所示。请回答下列问题:
2SO3(g)反应过程的能量变化如图所示。请回答下列问题:
(1)图中A表示 。
(2)E的大小对该反应的焓变有无影响? 。
该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低? 。
(3)某温度下,向1L密闭容器中开始充入2molSO2和1molO2,在V2O5催化剂存在时反应达到平衡,压强减小为开始时的
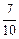 ;如在相同温度下,在同等体积的密闭容器中充入2mol的SO3,也在V2O5催化剂存在时反应达到平衡,求此温度下反应2SO3 (g)
;如在相同温度下,在同等体积的密闭容器中充入2mol的SO3,也在V2O5催化剂存在时反应达到平衡,求此温度下反应2SO3 (g) 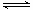 2SO2(g) + O2(g)的平衡常数(写出计算过程)
2SO2(g) + O2(g)的平衡常数(写出计算过程)(Ⅱ)化学试剂的生产和电镀工业排放的废水中常含有20~100mg.L-1Cr(Ⅵ),饮用含Cr(Ⅵ)的水会损害人的肠胃等,已知Cr(Ⅲ)的毒性是Cr(Ⅵ)的0.5%,国家规定工业废水含Cr(Ⅵ)的量排放标准为0.1mg.L-1。工业上常用化学法和电解法处理含Cr(Ⅵ)废水,再将Cr(Ⅲ)转化成沉淀除去,某研究性学习小组为研究废水的净化,设计了如下实验流程:

(1)配平第①步反应的离子方程式:
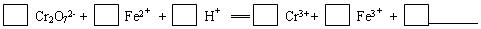
(2)第②步中用PH试纸测定溶液PH的操作是:
(3)设计一个电解装置也可以实现上述目的,装置如下图(用铁棒和石墨作电极):

电极材料:c为:
电极反应:d极:
Ⅰ. (1)反应物总能量 (1分)
(2)无 降低 (2分)
(3)设平衡时反应生成SO3的物质的量为2x mol
2SO2(g) + O2(g)
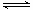 2SO3(g)
2SO3(g)开始量 2mol 1mol 0
反应转化量 2x mol x mol 2x mol
平衡量 (2-2x)mol (1-x)mol 2x mol
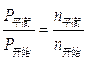
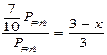 解得x="0.9" mol (2分)
解得x="0.9" mol (2分)同等条件下开始加入2molSO3与开始加入2molSO2、1molO2是相当的,属于等效平衡,平衡时各物质的浓度相等。
反应2SO3 (g)
 2SO2 (g) + O2(g) 的平衡常数:
2SO2 (g) + O2(g) 的平衡常数: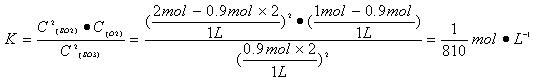
或1.2×10-3mol?L-1) (3分)
Ⅱ: (1) 1 6 14 2 6 7 H2O (2分)
(2)将一小块pH试纸放在表面皿上,用玻璃棒蘸取少量待测液,点在pH试纸上,再与标准比色卡对照,确定PH值。(2分)
(3)铁棒 2H+ + 2e - = H2↑ 或2H2O + 2e - = H2↑+2OH- (3分)
略

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目
 (l)+O2(g) △H= -196.46kJ·mol-1
(l)+O2(g) △H= -196.46kJ·mol-1 1
1
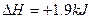 ·mol-1可知金刚石比石墨稳定
·mol-1可知金刚石比石墨稳定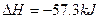 ·mol-1
·mol-1 O2(g);
O2(g);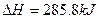 ·
· mol-1
mol-1