题目内容
断开1molAB(g)分子中的化学键使其分别生成气态A原子和气态B原子所吸收的能量称为A-B键的键能.下表列出了一些化学键的键能E:
请回答下列问题:
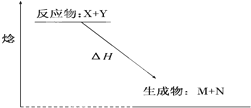
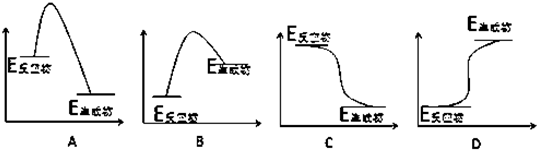
(1)如图表示某反应的能量变化关系,则此反应为______(填“吸热”或“放热”)反应,其中△H=______(用含有a、b的关系式表示).
(2)若图示中表示反应H2(g)+
O2(g)═H2O(g)△H=-241.8kJ?mol-1,则b=______kJ?mol-1,
x=______.
(3)历史上曾用“地康法”制氯气,这一方法是用CuCl2作催化剂,在450℃利用空气中的氧气跟氯化氢反应制氯气.反应的化学方程式为______.
若忽略温度和压强对反应热的影响,根据上题中的有关数据,计算当反应中有1mol电子转移时,反应的能量变化为______.

| 化学键 | H-H | Cl-Cl | O═O | C-Cl | C-H | O-H | H-Cl |
| E/kJ?mol-1 | 436 | 247 | x | 330 | 413 | 463 | 431 |
(1)如图表示某反应的能量变化关系,则此反应为______(填“吸热”或“放热”)反应,其中△H=______(用含有a、b的关系式表示).
(2)若图示中表示反应H2(g)+
| 1 |
| 2 |
x=______.
(3)历史上曾用“地康法”制氯气,这一方法是用CuCl2作催化剂,在450℃利用空气中的氧气跟氯化氢反应制氯气.反应的化学方程式为______.
若忽略温度和压强对反应热的影响,根据上题中的有关数据,计算当反应中有1mol电子转移时,反应的能量变化为______.

(1)由图可知反应物的总能量大于生成物的总能量,属于放热反应,焓变等于断开反应物中化学键吸收的能量减去形成生成物中化学键释放的能量,因此△H=(a-b) kJ?mol-1,
故答案为:放热;(a-b) kJ?mol-1;
(2)b为1mol水中含有的化学键的键能,即为2倍的O-H的键能,因此b=2×463kJ?mol-1=926kJ?mol-1,根据焓变△H=反应物的键能总和-生成物的键能总和可得:436+
-463×2=-241.8,求得x=496.4,
故答案为:926;496.4;
(3)用CuCl2作催化剂,在450℃利用空气中的氧气跟氯化氢反应制氯气,生成氯气和水,配平书写化学方程式为:O2+4HCl
2Cl2+2H2O,
O2(g)+4HCl(g)═2Cl2(g)+2H2O(g)△H=E(O=O)+4E(H-Cl)-2E(Cl-Cl)-4E(O-H)=(496.4+4×431-2×247-4×463)kJ?mol-1=-125.6 kJ?mol-1,
当1mol氧气完全反应时转移为4mol,放出125.6kJ热量,当1mol电子转移时放出的热量为:125.6kJ×
=31.4kJ,
故答案为:O2+4HCl
2Cl2+2H2O;放出能量31.4 kJ.
故答案为:放热;(a-b) kJ?mol-1;
(2)b为1mol水中含有的化学键的键能,即为2倍的O-H的键能,因此b=2×463kJ?mol-1=926kJ?mol-1,根据焓变△H=反应物的键能总和-生成物的键能总和可得:436+
| x |
| 2 |
故答案为:926;496.4;
(3)用CuCl2作催化剂,在450℃利用空气中的氧气跟氯化氢反应制氯气,生成氯气和水,配平书写化学方程式为:O2+4HCl
| ||
| 催化剂 |
O2(g)+4HCl(g)═2Cl2(g)+2H2O(g)△H=E(O=O)+4E(H-Cl)-2E(Cl-Cl)-4E(O-H)=(496.4+4×431-2×247-4×463)kJ?mol-1=-125.6 kJ?mol-1,
当1mol氧气完全反应时转移为4mol,放出125.6kJ热量,当1mol电子转移时放出的热量为:125.6kJ×
| 1 |
| 4 |
故答案为:O2+4HCl
| ||
| 催化剂 |

练习册系列答案
相关题目
 12CO2(g)+4CO(g)+18H2O(l)
12CO2(g)+4CO(g)+18H2O(l)