题目内容
14.分子式为C5H12O的戊醇共8种同分异构体,这些同分异构体若发生消去反应,生成烯烃的种类有( )| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
分析 根据能发生消去反应的醇是与羟基相连碳原子相邻的碳原子上至少有1个氢原子确定符合条件的醇,进而确定烯烃的种类.
解答 解:戊醇可能的结构有:HOCH2CH2CH2CH2CH3、HOCH(CH3)CH2CH2CH3、HOCH(CH2CH3)2、HOCH2CH(CH3)CH2CH3、HOC(CH3)2CH2CH3、HOCH(CH3)CH(CH3)2、HOCH2CH2CH(CH3)2、HOCH2C(CH3)3,能发生消去反应的有机化合物有HOCH2CH2CH2CH2CH3、HOCH(CH3)CH2CH2CH3、HOCH(CH2CH3)2、HOCH2CH(CH3)CH2CH3、HOC(CH3)2CH2CH3、HOCH(CH3)CH(CH3)2、HOCH2CH2CH(CH3)2,共7种,得到的消去产物分别为:CH2=CHCH2CH2CH3、CH3CH=CH2CH2CH3、CH=C(CH3)CH2CH3、C(CH3)2=CHCH3、CH2=CHCH(CH3)2,共5种,
故选B.
点评 本题考查同分异构体的书写,难度较大,注意能发生消去反应的醇是与羟基相连碳原子相邻的碳原子上至少有1个氢原子.

练习册系列答案
相关题目
11.下列装置、试剂选用或操作正确的是( )
| A. | 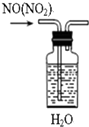 除去NO中的NO2 | B. | 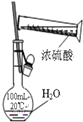 稀释浓硫酸 | ||
| C. |  实验室制取NH3 | D. | 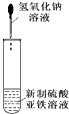 制备氢氧化亚铁并观察其颜色 |
5.某小组同学利用铝和氧化铁发生铝热反应后得到的固体进行如下实验.
(1)铝和氧化铁反应的化学方程式是2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe.
(2)固体成分的初步确定.
①由上述实验可知:溶液中Fe元素的存在形式有Fe2+、Fe3+.
②ⅰ中产生H2的原因是样品中除含Fe外,可能有未反应的Al,为检验样品中是否含Al单质,设计了相关实验,依据的原理是(用离子方程式表示)2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
③生成O2的化学方程式是2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑.
进一步的实验表明,上述固体样品中Fe元素的存在形式有:Fe、Fe2O3、Fe3O4.
(3)该小组同学对ⅱ中溶液红色褪去的原因做进一步探究.
提示:KSCN中S元素的化合价为-2价
①实验ⅲ中白色沉淀的化学式是BaSO4.
②结合实验ⅲ和ⅳ分析,实验ⅱ中红色褪去的原因是溶液中SCN-离子被H2O2氧化,溶液红色褪去.
③查阅资料得知:Cl-对溶液红色褪去的反应有催化作用,验证该说法应补充的实验和现象是分别取2mL0.1mol/LFeCl3溶液和2mL 0.05mol/L Fe2(SO4)3溶液,分别滴入KSCN溶液,溶液均变为红色;再分别加入等浓度等体积的H2O2溶液,FeCl3溶液褪色快(或取0.05mol/L Fe2(SO4)3溶液,滴入KSCN溶液,溶液变红色,将红色溶液分为2份,1份加入NaCl固体,另一份不变,向这两份溶液中均加入等浓度等体积的H2O2溶液,加入NaCl的溶液红色迅速褪色).
(1)铝和氧化铁反应的化学方程式是2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe.
(2)固体成分的初步确定.
| 实验序号 | 操作及现象 |
| ⅰ | 取少量固体样品,加入过量稀盐酸,固体溶解,产生无色气体(经检验为H2),溶液呈浅黄色 |
| ⅱ | 向ⅰ中所得溶液中加入少量KSCN溶液,溶液呈浅红色,再加入H2O2溶液至过量,产生无色气体(经检验为O2),溶液变为深红色,且红色很快褪去 |
②ⅰ中产生H2的原因是样品中除含Fe外,可能有未反应的Al,为检验样品中是否含Al单质,设计了相关实验,依据的原理是(用离子方程式表示)2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
③生成O2的化学方程式是2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑.
进一步的实验表明,上述固体样品中Fe元素的存在形式有:Fe、Fe2O3、Fe3O4.
(3)该小组同学对ⅱ中溶液红色褪去的原因做进一步探究.
| 实验序号 | 操作、现象 |
| ⅲ | 将ⅱ中剩余溶液均分为两份,一份滴加NaOH溶液,产生红褐色沉淀; 另一份滴加BaCl2溶液,产生白色沉淀,加入盐酸,沉淀不溶解 |
| ⅳ | 取2mL 0.1mol/L FeCl3溶液,滴入KSCN溶液,溶液变为红色,通入一段时间O2, 无明显变化.再加入H2O2溶液,红色很快褪去 |
①实验ⅲ中白色沉淀的化学式是BaSO4.
②结合实验ⅲ和ⅳ分析,实验ⅱ中红色褪去的原因是溶液中SCN-离子被H2O2氧化,溶液红色褪去.
③查阅资料得知:Cl-对溶液红色褪去的反应有催化作用,验证该说法应补充的实验和现象是分别取2mL0.1mol/LFeCl3溶液和2mL 0.05mol/L Fe2(SO4)3溶液,分别滴入KSCN溶液,溶液均变为红色;再分别加入等浓度等体积的H2O2溶液,FeCl3溶液褪色快(或取0.05mol/L Fe2(SO4)3溶液,滴入KSCN溶液,溶液变红色,将红色溶液分为2份,1份加入NaCl固体,另一份不变,向这两份溶液中均加入等浓度等体积的H2O2溶液,加入NaCl的溶液红色迅速褪色).
6.在钢铁腐蚀过程中,下列五种变化可能发生的是( )
①Fe2+转化为Fe3+ ②O2被还原 ③产生H2④Fe(OH)3失水形成Fe2O3•nH2O ⑤杂质碳被氧化.
①Fe2+转化为Fe3+ ②O2被还原 ③产生H2④Fe(OH)3失水形成Fe2O3•nH2O ⑤杂质碳被氧化.
| A. | 只有①和② | B. | 只有②③④ | C. | ①②③④ | D. | ①②③④⑤ |
3.在一定温度下将Cl2通入NaOH溶液中,得到ClO-、ClO3-等离子,其物质的量n(mol)随反应时间t(min)的变化如图所示.下列有关说法正确的是( )
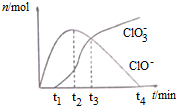

| A. | t1时,溶液中Na+、NH4+、CO32-、S2-可以大量共存 | |
| B. | t2时,溶液中含氯微粒浓度大小:c(ClO-)>c(Cl-)>c(ClO3-) | |
| C. | t3时,离子方程式为:4Cl2+8OH-=ClO3-+ClO-+6Cl-+4H2O | |
| D. | t4时,因c(ClO-)接近于0,所以c(ClO3-)=c(Cl-) |
4.下列说法正确的是( )
| A. | 乙烯和苯都能使溴水褪色,褪色的原因相同 | |
| B. | CH3-CH=CH-CH3与C3H6一定互为同系物 | |
| C. | 用浸泡过高锰酸钾溶液的硅藻土吸收水果释放的乙烯,可达到水果保鲜的目的 | |
| D. | C3H8的二氯代物共有3种 |
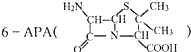 是青霉素类抗生素的母核,与有机物F缩合生成阿莫西林.某同学用对甲基苯酚为原料设计阿莫西林的合成路线如图:
是青霉素类抗生素的母核,与有机物F缩合生成阿莫西林.某同学用对甲基苯酚为原料设计阿莫西林的合成路线如图: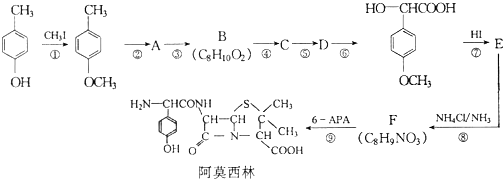
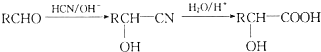
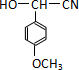 .
.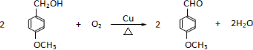 .
.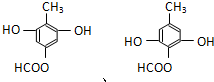 .
.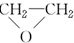 (环氧乙烷).
(环氧乙烷).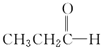 $\stackrel{NaBH_{4}}{→}$CH3CH2CH2OH
$\stackrel{NaBH_{4}}{→}$CH3CH2CH2OH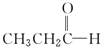 $→_{HCl}^{Zn(Hg)}$CH3CH2CH3
$→_{HCl}^{Zn(Hg)}$CH3CH2CH3