��Ŀ����
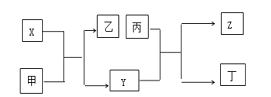
����Ŀ��ͭ���仯�����ڹ�ҵ��������������;��ij�����Ի�ͭ��(��Ҫ�ɷ�Ϊ Cu2S�������� Fe2O3��SiO2 ������)Ϊԭ���Ʊ�������ˮ�ļ�ʽ̼��ͭ���������£�

��֪��
�ٳ����¼������ʿ�ʼ�γɳ�������ȫ����ʱ��pH���±�
�������� | Fe2�� | Fe3�� | Cu2�� | Mn2�� |
��ʼ���� | 7.5 | 2.7 | 5.6 | 8.3 |
��ȫ���� | 9.0 | 3.7 | 6.7 | 9.8 |
�� Ksp[Fe(OH)3]��4.0��10��38
(1)�ӿ�����ȡ�����ʣ����ʵ���������Ũ���⣬���ɲ�ȡ�Ĵ�ʩ��__________����дһ�֣���
(2)����I�е���Ҫ�ɷ���MnO2��S��SiO2����д������ȡ����Ӧ������S�Ļ�ѧ����ʽ��______________��
(3)��������������ʱ������Լ�A����CuO�ȣ�����pH���ķ�ΧΪ_________������ A ����Һ�� pH��Ϊ4.0������Һ�� Fe3����Ũ��Ϊ_________mol/L��
(4)д����������(�� Mn2��)�����з�Ӧ�����ӷ���ʽ��_________________________��
(5)���ϰ���ʱ�������˵IJ���������________________��
(6)���ˢ�õ��ij�������ϴ�ӡ�������Եõ���ʽ̼��ͭ���жϳ����Ƿ�ϴ���IJ�����________________��
���𰸡���ֽ��裬����ͭ����飬���ȵ�(˵����������) 2MnO2+Cu2S+4H2SO4=S��+2CuSO4+2MnSO4+4H2O 3.7��5.6�� ��3.7��pH<5.6�� 4.0��10��8 Mn2����HCO3����NH3��MnCO3����NH4�� ����Һ���� ȡ�������һ��ϴ��Һ�ڽྻ���Թ��У���������ϡ�����ữ���ټ���BaCl2��Һ�����ް�ɫ������������˵��������ϴ������֮δϴ����������������Ҳ�ɣ�
��������
��ͭ����Ҫ�ɷ�ΪCu2S��������Fe2O3��SiO2�����ʣ�����ϡ����Ͷ������̽�ȡ�����˵õ�����ΪMnO2��SiO2������S����Һ�к���Fe3+��Mn2+��Cu2+��������ҺpH��ȥ�����ӣ�����̼�������Һ�����̹��˵õ���Һ�ϳ�����ѭ��ʹ�ã��õ���ʽ̼��ͭ���ݴ˷�������⡣
��1�����ʱ��ͨ����ֽ��裬����ͭ����飬���ȵȶ�������߽�ȡ�ʣ�
��2������ȡ��ʱ������������������MnO2����Cu2S�õ��������CuSO4��MnSO4���䷴Ӧ�Ļ�ѧ����ʽΪ��2MnO2+Cu2S+4H2SO4=S��+2CuSO4+2MnSO4+4H2O��
��3������������Ҫ�dz�ȥ��Һ��Fe3+��������ɱ����֪����ҪʹFe3+��ȫ������������Cu2+����Һ��pH��ΧΪ��3.7��5.6��3.7��pH<5.6������ҺpH=4����c(H+)=1��10-4mol/L��c(OH-)=![]() =
=![]() mol/L=1��10-10mol/L��c(Fe3+)=
mol/L=1��10-10mol/L��c(Fe3+)=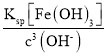 =
= 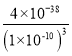 mol/L=4.0��10��8mol/L��
mol/L=4.0��10��8mol/L��
��4����������(��Mn2+)�����У�����̼����狀Ͱ���������̼���̳�������Ӧ�����ӷ���ʽΪ��Mn2����HCO3����NH3��MnCO3����NH4����
��5�����ϰ���ʱ�������˵IJ��������Ǽ�С�����ܽ�ȣ��������ӷ������壬�������ϣ�
�ʴ�Ϊ������Һ���ȣ�
��6������������Ҫ����Ϊ�����εȣ���˼�������Ƿ�ϴ���IJ���Ϊ��ȡ�������һ��ϴ��Һ�ڽྻ���Թ��У���������ϡ�����ữ���ټ���BaCl2��Һ�����ް�ɫ������������˵��������ϴ������֮δϴ����

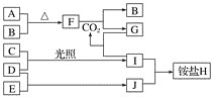
����Ŀ�����Բ��ϲ�ҵ��21���������չ�ĸ߿Ƽ�֧����ҵ֮һ�����Բ��Ϲ㷺���ڵ�����Ϣ�����¼���������̼������Ҫ�����Ʊ����������壬��ҵ�����Ȼ�隣����̿���Ʊ��ߴ���̼���̵Ĺ����������£�
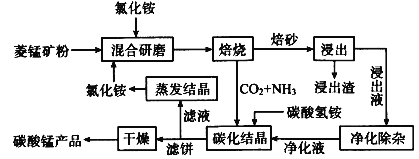
��֪�����̿�۵���Ҫ�ɷ���MnCO3����������Fe��Al��Ca��Mg��Ԫ�ء�
����ؽ���Mn+����c(Mn+)��0.1molL -1�γ�M(OH)n������pH��Χ���£�
�������� | Fe3+ | Al3+ | Fe2+ | Mg2+ | Ca2+ | Mn2+ |
��ʼ������pH | 1.5 | 3.8 | 6.3 | 9.6 | 10.6 | 8.8 |
������ȫ��pH | 2.8 | 5.2 | 8.3 | 11.6 | 12.6 | 10.8 |
�ش��������⣺
��1�������ա�ʱ��������Ҫ��Ӧ�Ļ�ѧ����ʽΪ___��
��2������Һ���������ӡ��������£��ټ���MnO2��Fe2+����ΪFe3+����__��Al3+��Fe3+��Ϊ������ȥ���ۼ���NH4F��__���ӳ�����ȥ��д����Ӧ�ٵ����ӷ���ʽΪ___��
��3��̼���ᾧʱ����Ӧ�����ӷ���ʽΪ___��
��4��̼���ᾧ�����в�����̼�����Һ����̼�������Һ���ܵ�ԭ����__����������ѭ�����õ����ʳ����Ȼ��֮���__��
��5���ⶨ̼���̲�Ʒ�Ĵ��ȡ�
��ȡ0.5000g̼���̲�Ʒ����ƿ�У���25.00mL���ᣬ���ȣ�̼����ȫ��ת��Ϊ[Mn(PO4)2]3-����ȴ�����¡���ˮϡ����100mL���μ�2��3��ָʾ����Ȼ����Ũ��Ϊ0.2000mol��L-1�����������[(NH4)2Fe(SO4)2]����Һ�ζ�����ӦΪ��[Mn(PO4)2]3- +Fe2+��Mn2+ +Fe3++2PO43-�����ظ�����3�Σ���¼�������±���
�ζ����� | 0.2000mol��L-1����������隣���Һ������mL�� | |
�ζ�ǰ | �ζ��� | |
1 | 0.10 | 20.20 |
2 | 1.32 | 21.32 |
3 | 1.05 | 20.95 |
���Ʒ�Ĵ���=__�����ζ��յ�ʱ���ֵζ��ܼ��촦���������ݣ����õ�̼���̴ֲ�Ʒ�Ĵ���__(�ƫ�ߡ���ƫ�͡�����Ӱ�족)��