题目内容
在熔融KOH中,大气中的氧可将铬铁矿(FeCr2O4)中Fe和Cr的化合价都转化为+6价,氧化1 mol FeCr2O4在理论上需要氧气( )
| A.2 mol | B.2.5 mol | C.3 mol | D.4 mol |
B
1 mol FeCr2O4中含Fe 1 mol,Cr 2 mol。在反应中,Fe的化合价由+2升到+6,Cr的化合价由+3升到+6,故两者共失去电子(6-2)×1 mol+(6-3)×2 mol="10" mol,根据得失电子守恒得n(O2)×4="10" mol,n(O2)=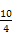 mol="2.5" mol。
mol="2.5" mol。
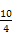 mol="2.5" mol。
mol="2.5" mol。
练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目


 Cl2↑+H2↑
Cl2↑+H2↑ Fe(OH)3+5OH-]
Fe(OH)3+5OH-]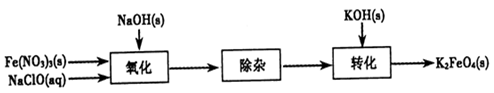
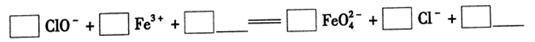
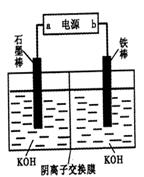
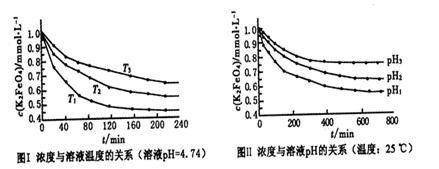
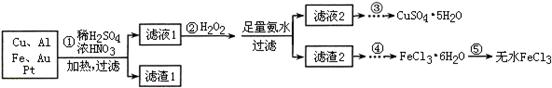
 2H2↑+O2↑,下列有关判断正确的是
2H2↑+O2↑,下列有关判断正确的是