题目内容
【题目】黄铁矿![]() 主要成分
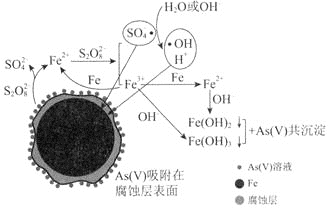
主要成分![]() 是工业制硫酸的主要原料,暴露在空气中会被缓慢氧化,其氧化过程如图所示。下列有关说法不正确的是
是工业制硫酸的主要原料,暴露在空气中会被缓慢氧化,其氧化过程如图所示。下列有关说法不正确的是

A.发生反应a时,![]() 被氧化时消耗标准状况下空气的体积大约
被氧化时消耗标准状况下空气的体积大约![]()
B.为了验证b溶液中含![]() ,可选用KSCN溶液和氯水
,可选用KSCN溶液和氯水
C.取10 mL b溶液测定其成分,通入标准状况下![]() 22.4 mL恰好完全反应。然后调节pH,使溶液中的铁元素全部转化为沉淀,经过滤、洗涤、灼烧,冷却后称重,得固体质量为0.32g,则b溶液中
22.4 mL恰好完全反应。然后调节pH,使溶液中的铁元素全部转化为沉淀,经过滤、洗涤、灼烧,冷却后称重,得固体质量为0.32g,则b溶液中![]()
D.现有一含有![]() 和
和![]() 的混合样品,采用一定方法测得
的混合样品,采用一定方法测得![]() ,则该样品中
,则该样品中![]() 的物质的量分数为
的物质的量分数为![]()
【答案】B
【解析】
A.![]() 被氧化生成
被氧化生成![]() ,
,![]() 被氧化时转移电子的物质的量为
被氧化时转移电子的物质的量为![]() ,需要氧气的物质的量为
,需要氧气的物质的量为![]() ,氧气在空气中的体积分数约为
,氧气在空气中的体积分数约为![]() ,则消耗标准状况下空气的体积大约为
,则消耗标准状况下空气的体积大约为![]() ,故A正确;
,故A正确;
B.b溶液中含有![]() 离子,用KSCN溶液和氯水无法说明溶液含有
离子,用KSCN溶液和氯水无法说明溶液含有![]() ,故B错误;
,故B错误;
C.![]() 固体为
固体为![]() ,
,![]() ,根据Fe元素守恒有:
,根据Fe元素守恒有:![]() ,故
,故![]() ,
,![]() ,故C正确;
,故C正确;
D.设![]() 的物质的量为x,
的物质的量为x,![]() 的物质的量为y,
的物质的量为y,![]() ,故
,故![]() ,故x:
,故x:![]() ,故
,故![]() 的物质的量分数为
的物质的量分数为![]() ,故D正确;
,故D正确;
故答案选B。

练习册系列答案
相关题目