题目内容
【题目】右表为元素周期表的一部分,其中X、Y、Z、W为短周期元素,Z元素的核电荷数为X与Y元素核电荷数之和。下列说法正确的是

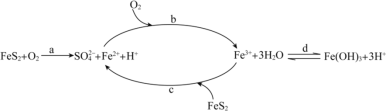
A.氢化物稳定性Y比W强,是因为Y的氢化物中存在氢键
B.XY2、XW2、ZY2熔沸点依次增大,都是由共价键形成的分子晶体
C.一定条件下,X单质能与ZY2反应生成Z单质,说明X的非金属性比Z强
D.根据元素周期律,可以推测T元素的单质具有半导体特性,钠能与T形成Na2T2化合物
【答案】D
【解析】
设X的原子序数为a,则Z的序数为a+8,Y恶序数为a+2,Z元素的核电荷数为X与Y元素核电荷数之和,则=" a+8=a+" a+2,a=6;所以X为碳元素、Y为氧元素、Z为硅元素、W为硫元素、T为硒元素;
根据上述分析可知,
A. 氢化物的稳定性与氢键无关,故A错误;
B. 二氧化硅是原子晶体,故B错误;
C. 一定条件下,碳单质能与二氧化硅反应生成硅单质,碳表现还原性,不能说明X的非金属性比Z强,,故C错误;
D. 硒元素在金属与非金属的分界线附近,硒与氧元素同族,根据元素周期律,可以推测硒元素的单质具有半导体特性,钠能与硒形成Na2Se2化合物,故D正确;
答案选D。

【题目】若反应 CO(g)+2H2(g)![]() CH3OH(g)在温度不变且体积恒定为1的密闭容器中发生,反应过程中各物质的物质的量随时间变化如表所示:
CH3OH(g)在温度不变且体积恒定为1的密闭容器中发生,反应过程中各物质的物质的量随时间变化如表所示:
时间/min | 0 | 5 | 10 | 15 |
H2 | 4mol | 2mol | ||
CO | 2mol | 1mol | ||
CH3OH(g) | 0 | 0.7mol |
①下列各项能作为判断该反应达到平衡标志的是____________(填字母);
A.容器内压强保持不变
B.2v正(H2)=v逆(CH3OH)
C.混合气体的相对分子质量保持不变
D.混合气体的密度保持不变
②若起始压强为P0 kPa,则在该温度下反应的平衡常数Kp=_________ (kPa)-2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
③反应速率若用单位时间内分压的变化表示,则10min内H2的反应速率v(H2)=__________kPamin-1。