题目内容
对于反应2SO2+O2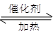 2SO3下列判断正确的是
2SO3下列判断正确的是
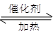 2SO3下列判断正确的是
2SO3下列判断正确的是| A.2 mol SO2和足量的O2反应,必生成2 mol SO3 |
| B.平衡时SO2、O2、SO3的分子数之比为2∶1∶2 |
| C.平衡时SO2的消耗速率必定等于O2的生成速率的2倍 |
| D.平衡时SO2的浓度必为O2浓度的2倍 |
C
试题分析:A.由于该反应是可逆反应,反应不可能完全进行,所以2 mol SO2和足量的O2反应,产生的SO3的物质的量必然小于2 mol。错误。B.物质在反应变化时这几种物质的SO2、O2、SO3的分子数之比为2∶1∶2,但是平衡时不一定是这种关系。错误。C.因为在平衡时任何物质的消耗速率与产生速率相同。在任何时刻SO2的消耗速率必定等于O2的消耗速率的2倍。SO2的消耗速率等于O2生成速率的2倍,则说明O2的消耗速率等于O2生成速率,因此反应达到平衡状态。正确。D.如果起始加入的SO2、O2的物质的量的比为2:1,因为在反应过程中二者的消耗的比为2:1,所以平衡时SO2的浓度为O2浓度的2倍。若加入的比例不是2:1,则达到平衡时SO2的浓度就不是O2浓度的2倍。错误。

练习册系列答案
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
 2AB(g) ,反应达到平衡状态的标志是
2AB(g) ,反应达到平衡状态的标志是  pC(g)+qQ(g)当m、n、p、q为任意整数时,达到平衡的标志是( )
pC(g)+qQ(g)当m、n、p、q为任意整数时,达到平衡的标志是( ) CH3OH(g)
CH3OH(g) 2SO3(g),混合体系中SO3的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:
2SO3(g),混合体系中SO3的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题: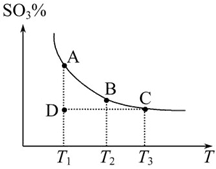
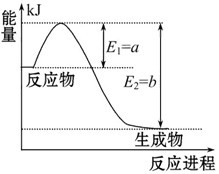
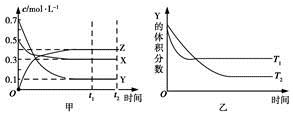
 2Z(g) ΔH>0
2Z(g) ΔH>0 CH3OH(g) +H2O(g) △H
CH3OH(g) +H2O(g) △H
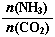 =3,达平衡时CO2的转化率为60%,则NH3的平衡转化率为: 。
=3,达平衡时CO2的转化率为60%,则NH3的平衡转化率为: 。 pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的一半,当达到新平衡时,C的浓度为原来1.9倍,下列说法错误的是
pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的一半,当达到新平衡时,C的浓度为原来1.9倍,下列说法错误的是