题目内容
(24分)下表是元素周期表的一部分, 针对表中的①~⑨种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是: (写元素符号)该原子结构示意图为 。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是 ,碱性最强的化合物的化学式是: 。
(3)最高价氧化物是两性氧化物的元素是 ;写出它的氧化物与氢氧化钠溶液反应的离子方程式 。
(4)形成的单质硬度最大的元素是 该单质的晶体类型为
(5)用电子式表示元素④与⑥形成的化合物: ,该化合物属于 化合物。(填 “共价”或“离子”)
(6)元素①与⑦形成的最简单的化合物的电子式是 。该化合物属于 化合物。(填 “共价”或“离子”)
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | | | | ① | ② | ③ | | |
| 3 | ④ | | ⑤ | | | ⑥ | ⑦ | ⑧ |
| 4 | ⑨ | | | | | | | |
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是 ,碱性最强的化合物的化学式是: 。
(3)最高价氧化物是两性氧化物的元素是 ;写出它的氧化物与氢氧化钠溶液反应的离子方程式 。
(4)形成的单质硬度最大的元素是 该单质的晶体类型为
(5)用电子式表示元素④与⑥形成的化合物: ,该化合物属于 化合物。(填 “共价”或“离子”)
(6)元素①与⑦形成的最简单的化合物的电子式是 。该化合物属于 化合物。(填 “共价”或“离子”)
(1) Ar (2) HClO4 KOH
(3) Al Al2O3+2OH-=2AlO2-+H2O (4) C 原子晶体
(5) 离子 (6)
离子 (6) 共价
共价
(3) Al Al2O3+2OH-=2AlO2-+H2O (4) C 原子晶体
(5)
 离子 (6)
离子 (6) 共价
共价考查元素周期表的结构和元素周期律的应用。根据元素在周期表中的位置可判断,①~⑨分别是C、N、O、Na、Al、S、Cl、Ar、K。
(1)稀有气体元素的最外层已经达到8电子稳定结构,其化学性质最不活泼。
(2)非金属性越强,最高价氧化物水化物的酸性越强,金属性越强,最高价氧化物水化物的碱性越强。同周期元素自左向右金属性逐渐减弱,非金属性逐渐增强。同主族元素自上而下金属性逐渐增强,非金属性逐渐减弱。所以最活泼的金属是K,非金属是Cl。
(3)氢氧化铝是两性氢氧化物,能溶于强碱氢氧化钠溶液中,方程式为Al2O3+2OH-=2AlO2-+H2O。
(4)金刚石的硬度增大,形成的晶体是原子晶体。
(5)钠是活泼的金属性元素,和硫形成的化学键是离子键,硫化钠的电子式为 。
。
(6)碳和氯都是非金属元素,形成的化学键是极性键,其化合物是共价化合物,电子式为
(1)稀有气体元素的最外层已经达到8电子稳定结构,其化学性质最不活泼。
(2)非金属性越强,最高价氧化物水化物的酸性越强,金属性越强,最高价氧化物水化物的碱性越强。同周期元素自左向右金属性逐渐减弱,非金属性逐渐增强。同主族元素自上而下金属性逐渐增强,非金属性逐渐减弱。所以最活泼的金属是K,非金属是Cl。
(3)氢氧化铝是两性氢氧化物,能溶于强碱氢氧化钠溶液中,方程式为Al2O3+2OH-=2AlO2-+H2O。
(4)金刚石的硬度增大,形成的晶体是原子晶体。
(5)钠是活泼的金属性元素,和硫形成的化学键是离子键,硫化钠的电子式为
 。
。(6)碳和氯都是非金属元素,形成的化学键是极性键,其化合物是共价化合物,电子式为


练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
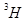 2O和
2O和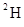 2O
2O 周期
周期