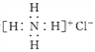题目内容
【题目】一定温度下在容积为5L的密闭容器中,通入5 molN2和8 molH2,在一定条件下反应生成NH3,当反应进行到2 min时,测得容器内有4 molNH3。则:
(1)求2 min内,H2的平均反应速率。_____
(2)求2min时N2的转化率。______
(3)2 min时,求容器内气体的压强与反应前气体压强的比值。(不用写计算过程)___
【答案】0.6mol·L-1·min-1 40% 9:13
【解析】
根据化学方程式
N2+3H2![]() 2NH3
2NH3
起始量(mol) 5 8 0
转化量(mol) 2 6 4
2min后(mol) 3 2 4
(1)H2的物质的量的变化是6mol,反应速率v(H2)=△c/△t=![]() = 0.6mol·L-1·min-1,故答案为:0.6mol·L-1·min-1。
= 0.6mol·L-1·min-1,故答案为:0.6mol·L-1·min-1。
(2)转化率=![]() ,故N2的转化率是
,故N2的转化率是![]() ×100%=40%,故答案为:40%。
×100%=40%,故答案为:40%。
(3)密闭容器的压强比等于气体的物质的量之比,反应前气体的物质的量是5+8=13mol,反应后气体的物质的量是3+2+4=9mol,容器内气体的压强与反应前气体压强的比值是9:13,故答案为:9:13。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目