题目内容
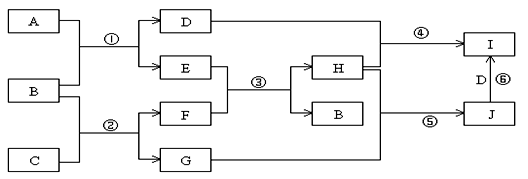
某研究性学习小组设计了一组实验来探究元素周期律。甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成N、C、Si三种非金属元素的非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证卤族元素性质的递变规律。A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润红纸。已知常温下浓盐酸与高锰酸钾能反应生成氯气。
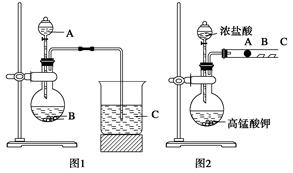
(1)甲同学设计实验的依据是____________________________________;
写出选用物质的名称:A____________,B__________,C____________;
上述反应的离子方程式分别为________________________________;
____________________________________________________________。
(2)乙同学的实验原理是__________________________________ 。
写出B处的离子方程式: _______________________________________。

(1)甲同学设计实验的依据是____________________________________;
写出选用物质的名称:A____________,B__________,C____________;
上述反应的离子方程式分别为________________________________;
____________________________________________________________。
(2)乙同学的实验原理是__________________________________ 。
写出B处的离子方程式: _______________________________________。
(1)强酸制弱酸(2分) 稀硝酸 碳酸钙 硅酸钠溶液(3分) CaCO3+2H+===Ca2++2CO2↑+H2O,(2分)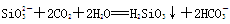 (2分)
(2分)
(2)强氧化剂生成弱氧化剂或活泼的非金属单质置换较不活泼的非金属单质(2分) 2I-+Cl2===2Cl-+I2(2分)
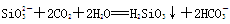 (2分)
(2分)(2)强氧化剂生成弱氧化剂或活泼的非金属单质置换较不活泼的非金属单质(2分) 2I-+Cl2===2Cl-+I2(2分)
试题分析:(1)根据甲设计的实验装置图可知,其实验的原理是利用较强酸制较弱酸。实验A、B、C中的试剂分别是稀硝酸、碳酸钙、硅酸钠溶液,有关反应的离子方程式分别是CaCO3+2H+===Ca2++2CO2↑+H2O、
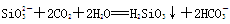 。
。(2)要验证卤族元素性质的递变规律,则可以利用活泼的非金属单质置换较不活泼的非金属单质来实现。酸性高锰酸钾溶液能把盐酸氧化生成氯气,所以B处反应的离子方程式是2I-+Cl2===2Cl-+I2。
点评:该题是中等难度试题的考查,试题注重基础,侧重能力和方法的考查和训练。该类试题综合性强,理论和实践的联系紧密,有的还提供一些新的信息,这就要求学生必须认真、细致的审题,联系所学过的知识和技能,进行知识的类比、迁移、重组,全面细致的思考才能得出正确的结论。

练习册系列答案
相关题目
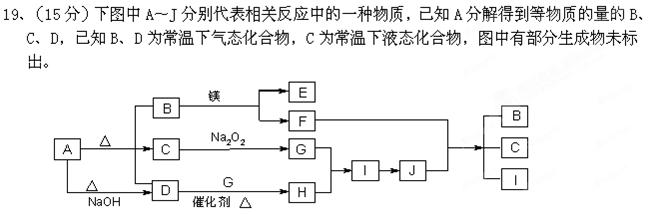
 B+镁 → E + F
B+镁 → E + F  。
。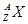 ,它的氯化物XCl2 2.22g溶于水制成溶液后,加入2mol/L的
,它的氯化物XCl2 2.22g溶于水制成溶液后,加入2mol/L的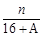 (A-N+8)mol
(A-N+8)mol (A-N+6)mol
(A-N+6)mol ,并且存
,并且存 在如下转换关系:
在如下转换关系:
 原剂的质量比为 。
原剂的质量比为 。