题目内容
14.以下对核外电子运动状况的描述正确的是( )| A. | 同一原子中,2p,3p,4p能级的轨道依次增多 | |
| B. | 当碳原子的核外电子排布由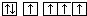 转变为 转变为 这一过程释放能量 这一过程释放能量 | |
| C. | 3p2表示3p能级有两个轨道 | |
| D. | 在同一能级上运动的电子,其运动状态可能相同 |
分析 A.同种能级含有的轨道数相同;
B.原子由激发态变为基态要放出能量;
C.3p2表示3p能级有2个电子;
D.在同一能级上运动的电子,其运动状态不同.
解答 解:A.同一原子中,不同能层,相同能级的轨道数相同,故A错误;
B.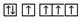 为激发态,能量较高,
为激发态,能量较高,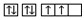 为基态,原子由激发态变为基态要放出能量,故B正确;
为基态,原子由激发态变为基态要放出能量,故B正确;
C.3p2表示3p能级有2个电子,但p能级有3个轨道,故C错误;
D.在同一能级上运动的电子,其运动状态不同,故D错误.
故选B.
点评 本题考查原子核外电子的运动和排布特点,题目难度不大,注意D项,为易错点,同一能级的电子,可在不同轨道运动,如在同一轨道,则电子的自旋方向不同.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.下列各种烷烃进行一氯取代反应后,只能生成三种沸点不同的有机产物的是( )
| A. | CH3CH2CH3 | B. | (CH3)2CHCH2CH3 | C. | CH3CH2CH2CH3 | D. | CH3(CH2)4CH3 |
5.某烃1mol完全燃烧生成4molCO2,且能与2mol氢气加成,该烃是下列中的( )
| A. | CH2=CHCH2CH3 | B. | (CH3)2CHCH=CH2 | C. | CH2=CH-CH=CH2 | D. | 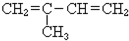 |
2.下列说法不正确的是( )
| A. | CH3-CH=CH2和CH2=CH2的最简式相同 | |
| B. | 乙二醇和丙三醇为同系物 | |
| C. | CH≡CH和C6H6含碳量相同 | |
| D. | 2-甲基-2-丙醇不能被催化氧化成相应的醛 |
9.设NA为阿伏加德罗常数,下列叙述中正确的是( )
| A. | 12.4g白磷晶体中含有的P-P键数是0.4NA | |
| B. | 7.8 g Na2S和Na2O2的混合物中含有的阴离子数大于0.1NA | |
| C. | 2 mol SO2和1 molO2在一定条件下的密闭容器中反应,反应后分子总数大于2 NA | |
| D. | 1mol甲醇中含有C-H键的数目为4NA |
19.下列叙述中正确的是( )
| A. | 同温同压下,相同体积的物质,所含的粒子数必相等 | |
| B. | 任何条件下,等质量的乙烯和一氧化碳所含的分子数必相等 | |
| C. | 1 L一氧化碳气体的质量一定比1 L氧气的质量小 | |
| D. | 等体积、等物质的量浓度的强酸中所含的H+数目一定相等 |
6.微粒甲与离子乙在溶液中的转化关系如图所示:微粒甲是( )


| A. | Si | B. | Na+ | C. | Al | D. | SO2 |
3.它们的氯化物的化学式,最可能正确的是( )
| A. | QCl2 | B. | RCl | C. | SCl3 | D. | TCl |