题目内容
【题目】香豆素-4是一种激光染料,应用于可调谐染料激光器。香豆素-4由C、H、O三种元素组成,分子球棍模型如图所示。下列有关叙述正确的是

①分子式为![]()
②能与饱和溴水发生取代反应
③能与饱和溴水发生加成反应
④能使酸性![]() 溶液褪色
溶液褪色
⑤1mol香豆素-4最多能与含1molNaOH的溶液反应
A. ①②③ B. ③④⑤ C. ②③④ D. ②③④⑤
【答案】C
【解析】①先将球棍模型转化为结构简式.根据碳有四价,氢有一价,氧有二价,氮有三价,画出该有机物的结构简式,得出分子式为C10H8O3,①错误;②香豆素-4中含有酚羟基,苯环能与溴水发生取代反应,②正确;③香豆素-4中含有碳碳双键,能与溴水发生加成反应,③正确;④香豆素-4中含有碳碳双键,酚羟基,都能被酸性KMnO4溶液氧化而使溶液褪色,④正确;⑤1mol酚羟基消耗1mol氢氧化钠;1mol羧基消耗1mol氢氧化钠;若有酯的结构,则先让酯进行酸性水解,再看产物能否和氢氧化钠反应:若酸性水解的产物是羧酸和醇,1mol酯只能和1mol氢氧化钠反应;若酸性水解的产物是羧酸和酚类物质,则1mol酯能和2mol氢氧化钠反应,所以根据酚羟基、酯基推断香豆素-4最多能与含3 mol NaOH的溶液反应,⑤错误;答案选C。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】(1)科学家寻找高效催化剂,通过如下反应实现大气污染物转化:
2CO(g) +2NO(g) ![]() N2(g)+2CO2(g) △H1
N2(g)+2CO2(g) △H1
已知:CO的燃烧热△H2=-283kJ/moL
N2(g) +O2(g) =2NO(g)几种化学键的键能数据如下:
化学键 | N≡N键 | O=O键 | NO中氮氢键 |
键能(kJ/mol) | 945 | 498 | 630 |
求△H1__________________。
(2)NH3作为一种重要化工原料,被大量应用于工业生产,与其有关性质反应的催化剂研究曾被列入国家863计划,在恒温恒容装置中充入一定量的NH3和O2,在某催化剂的作用下进行下述反应I,测得不同时间的NH3和O2的浓度如下表:
时间(min) | 0 | 5 | 10 | 15 | 20 | 25 |
C(NH3)/mol·L-1 | 1.00 | 0.36 | 0.12 | 0.08 | 0. 0072 | 0.0072 |
C(O2)/mol·L-1 | 2.00 | 1.20 | 0.90 | 0.85 | 0.84 | 0.84 |
则下列有关叙述中正确的是______________
A.使用催化剂时,可降低该反应的活化能,加快其反应速率
B. 若测得容器内4v正(NH3)=6v逆(H2O)时,说明反应已达平衡
C.当容器内![]() =1时,说明反应已达平衡
=1时,说明反应已达平衡
D.前10分钟内的平均速率v(NO)=0.088mol·L-1·min-1
<>(3)氨催化氧化时会发生下述两个竞争反应I、II。催化剂常具有较强的选择性,即专一性。已知:反应I 4NH3(g)+5O2(g)![]() 4NO(g) +6H2O(g)
4NO(g) +6H2O(g)
反应 II:4NH3(g)+3O2(g) ![]() 2N2(g) +6H2O(g)
2N2(g) +6H2O(g)
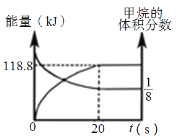
为分析某催化剂对该反应的选择性,在1L密闭容器中充入1 mol NH3和2mol O2,测得有关物质的量关系如图:

①该催化剂在高温时选择反应____________ (填“ I ”或“ II”)。
② 520℃时,4NH3(g)+3O2![]() 4N2(g) +6H2O(g)的平衡常数K=________________ (不要求得出计算结果,只需列出数字计算式)。
4N2(g) +6H2O(g)的平衡常数K=________________ (不要求得出计算结果,只需列出数字计算式)。
③由图像可判断,反应I正反应△H_______________ 0(填“>”、“<”,或“=”)
④C点比B点所产生的NO的物质的量少的主要原因_________________________。
(4)羟胺(NH2OH)的电子式_____________,羟胺是一种还原剂,可用作显像剂还原溴化银生成银单质和氮气,该反应的化学方程式为______________________________。
现用25.00mL0.049mol/L的羟胺的酸性溶液跟足量的硫酸铁溶液在煮沸条件下反应,生成的Fe2+恰好与24.50mL 0.020mol/L的KMnO4酸性溶液完全作用,则在上述反应中,羟胺的氧化产物是_____。