题目内容
(1)相同物质的量浓度下的各溶液:NaX、NaY、NaZ,其PH值依次为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序为:
(2)将AlCl3溶于水后,经加热蒸发、蒸干,灼烧,最后所得白色固体的主要成分是
(3)把a、b、c、d四种金属片浸泡在稀硫酸中,用导线两两相连,可以组成各种原电池.若a b相连,a为负极;c d相连,c为负极;a c相连,c为正极;b d相连,b为正极,则四种金属的活动性由强到弱顺序为:
(4)写出Na2CO3溶于水后的电离方程式:
(5)写出氯化铁溶液水解反应的离子方程式
HX>HY>HZ
HX>HY>HZ
(2)将AlCl3溶于水后,经加热蒸发、蒸干,灼烧,最后所得白色固体的主要成分是
Al2O3
Al2O3
(3)把a、b、c、d四种金属片浸泡在稀硫酸中,用导线两两相连,可以组成各种原电池.若a b相连,a为负极;c d相连,c为负极;a c相连,c为正极;b d相连,b为正极,则四种金属的活动性由强到弱顺序为:
a>c>d>b
a>c>d>b
(4)写出Na2CO3溶于水后的电离方程式:
Na2CO3=2Na++CO32-
Na2CO3=2Na++CO32-
(5)写出氯化铁溶液水解反应的离子方程式
Fe3++3H2O?Fe(OH)3+3H+
Fe3++3H2O?Fe(OH)3+3H+
.分析:(1)根据酸根离子水解程度越大,对应的酸越弱来解答;
(2)先判断是否水解及水解产物,再根据水解产物判断灼烧时的分解产物;
(3)原电池中,负极材料为较活泼的金属,发生氧化反应,正极为较不活泼的金属,发生还原反应,以此判断金属的活动性;
(4)碳酸钠属于强电解质,能完全电离;
(5)三价铁离子水解生成氢氧化铁和氢离子.
(2)先判断是否水解及水解产物,再根据水解产物判断灼烧时的分解产物;
(3)原电池中,负极材料为较活泼的金属,发生氧化反应,正极为较不活泼的金属,发生还原反应,以此判断金属的活动性;
(4)碳酸钠属于强电解质,能完全电离;
(5)三价铁离子水解生成氢氧化铁和氢离子.
解答:解:(1)因pH越大,说明酸根离子水解越是强烈,对应的酸越弱.所以HX、HY、HZ的酸性由强到弱的顺序:HX>HY>HZ,故答案为:HX>HY>HZ;
(2)AlCl3是强酸弱碱盐,能水解生成氢氧化铝和氯化氢,AlCl3+3H2O?Al(OH)3+3HCl,HCl具有挥发性,所以在加热蒸发、蒸干,灼烧过程中挥发消失;灼烧Al(OH)3,Al(OH)3能分解生成氧化铝和水2Al(OH)3
Al2O3+3H2O,水在加热过程中蒸发掉,所以最后得到的白色固体是Al2O3,故答案为:Al2O3;
(3)若a.b相连时,a为溶解,则a为负极,活动性a>b;c.d相连时c为负极,活动性c>d;a.c相连时c为正极,a为负极,活动性a>c;b.d相连时b为正极,d为负极,活动性d>b;则有活动性a>c>d>b,
故答案为:a>c>d>b;
(4)碳酸钠属于强电解质,溶于水后能完全电离:Na2CO3=2Na++CO32-,故答案为:Na2CO3=2Na++CO32-;
(5)三价铁离子的水解原理为:Fe3++3H2O?Fe(OH)3+3H+,故答案为:Fe3++3H2O?Fe(OH)3+3H+.
(2)AlCl3是强酸弱碱盐,能水解生成氢氧化铝和氯化氢,AlCl3+3H2O?Al(OH)3+3HCl,HCl具有挥发性,所以在加热蒸发、蒸干,灼烧过程中挥发消失;灼烧Al(OH)3,Al(OH)3能分解生成氧化铝和水2Al(OH)3
| ||
(3)若a.b相连时,a为溶解,则a为负极,活动性a>b;c.d相连时c为负极,活动性c>d;a.c相连时c为正极,a为负极,活动性a>c;b.d相连时b为正极,d为负极,活动性d>b;则有活动性a>c>d>b,
故答案为:a>c>d>b;
(4)碳酸钠属于强电解质,溶于水后能完全电离:Na2CO3=2Na++CO32-,故答案为:Na2CO3=2Na++CO32-;
(5)三价铁离子的水解原理为:Fe3++3H2O?Fe(OH)3+3H+,故答案为:Fe3++3H2O?Fe(OH)3+3H+.
点评:本题重点考查学生盐的水解规律以及水解方程式的书写问题,注意知识的积累是解题关键,难度不大.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
下列说法正确的是( )
| A、一定条件反应:2CO(g)?CO2(g)+C(s)可自发进行,则该反应的△H>0 | B、向硫酸亚铁溶液中滴加硫氰化钾溶液产生血红色沉淀说明溶液已变质 | C、在反应KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O中,当生成1.5mol Cl2时,反应中转移的电子数为2.5NA | D、相同物质的量浓度的下列溶液:①NH4HSO4②NH4Cl③NH3?H2O,水电离程度由大到小的顺序是:①>②>③ |
(21分)(1)用50mL 0.55mol/L NaOH溶液和50mL 0.25mol/L H2SO4溶液来做中和热测定的实验,测得溶液在反应前后的温度变化为t1℃~t2℃(t2>t1),混合后溶液的比热容为c = 4.18J/(g·℃),溶液的密度都近似为1g/mL,中和热△H=__________(填表达式,不用化简);若将H2SO4溶液换成相同物质的量浓度的CH3COOH溶液,测得的△H______填(“偏大”、“偏小”或“相同”);若将稀硫酸换成浓硫酸来做该实验,测得的△H_______(填“偏大”、“偏小”或“相同”)。
(2)某高能化学物质N2H2内,氮元素的杂化类型为____,电子式为____,一个分子中有σ键 个 ,π 键 个。
(3).在密闭容器中进行可逆反应: CO(g)+NO2(g) CO2(g)+NO(g),(正反应放热),达到平衡后,只改变其中一个条件,对平衡的影响是:
CO2(g)+NO(g),(正反应放热),达到平衡后,只改变其中一个条件,对平衡的影响是:
①增大容器的体积,平衡 移动(填“正向”“逆向”“不”),反应混合物的颜色 。(填“变深”“变浅”“不变”)
②容器体积不变:若通人CO2气体,平衡 移动,反应混合物的颜色 。若通人N2气体,平衡 移动,反应混合物的颜色 。③加入催化剂,平衡 移动。
(4)下表是几种常用燃料(1 mol)完全燃烧时放出的热量:
| 物质 | 炭粉(C) | 一氧化碳(CO) | 氢气(H2) | 甲烷(CH4) | 乙醇(C2H5OH) |
| 状态 | 固体 | 气体 | 气体 | 气体 | 液体 |
| 热量(kJ) | 392.8 | 282.6 | 285.8 | 890.3 | 1 367 |
②写出管道煤气中的一氧化碳燃烧热的热化学方程式_______________________
③充分燃烧1 mol表中各种燃料,排放出二氧化碳的量最多的是________。
④矿物燃料储量有限,而且在燃烧过程中会产生污染。根据能源多样化的发展战略,我国开发利用的绿色能源有________等。
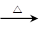 (化学方程式)
。
(化学方程式)
。