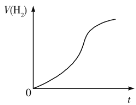
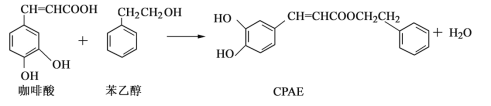
题目内容
【题目】常温下,向1LpH=10的NaOH溶液中持续通入CO2。通入的CO2的体积(V)与溶液中水电离出的OH-离子浓度(φ)的关系如图所示。下列叙述正确的是
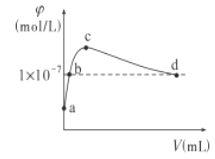
A.a点溶液中:水电离出的c(H+)=1×10-10mol/L
B.b点溶液中:n(Na+)=1×10-10mol
C.c点溶液中:c(Na+)>c(![]() )>c(
)>c(![]() )
)
D.d点溶液中:c(Na+)=2c(![]() )+c(
)+c(![]() )
)
【答案】AD
【解析】
A.a点溶液为1LpH=10的NaOH溶液,溶液中氢离子浓度为1×10-10mol·L-1,就是水电离出的,故A正确;
B.b点溶液中的钠离子全部来自于1LpH=10的NaOH溶液,故![]() ,故B错误;
,故B错误;
C.c点溶液中水电离出的氢氧根离子浓度最大,说明溶液为碳酸钠,根据碳酸根要水解,离子在溶质中出现在前,不出现在后分析,溶液中离子浓度关系为:c(Na+)>c(CO32-)>c(HCO3-),故C错误;
D.d点溶液为碳酸氢钠和碳酸的混合液,此时溶液呈中性,电荷守恒为c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-),c(OH-)= c(H+)=1×10-7mol·L-1,则:c(Na+)=2c(CO32-)+c(HCO3-),故D正确。
故选AD。

练习册系列答案
相关题目
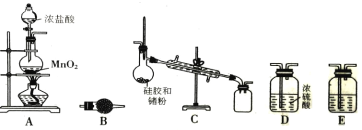
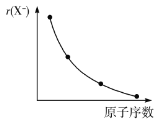
【题目】下列图像能说明或反映其对应关系的是( )
|
|
|
|
A | B | C | D |
A.第二周期元素的化合价变化
B.第ⅦA族元素简单阴离子的半径变化
C.向50 mL 0.5mol·L-1NaOH溶液中逐滴加入等浓度盐酸时溶液的pH变化
D.Al与稀硫酸反应产生H2的体积变化