题目内容
【题目】硼(B)及其化合物在化学工业中有诸多用途。请回答下列问题:
(1)硼氢化钠(NaBH4)是硼的重要化合物。
①NaBH4中B元素的化合价为___。
![]() 工业上可利用硼酸甲酯[B(OCH3)3]与氢化钠(NaH)反应制备NaBH4,反应的另一种产物为甲醇钠(CH3ONa),该反应的化学方程式为___。NaBH4与水反应生成NaBO2和H2,该反应生成的氧化产物与还原产物的物质的量之比为___。
工业上可利用硼酸甲酯[B(OCH3)3]与氢化钠(NaH)反应制备NaBH4,反应的另一种产物为甲醇钠(CH3ONa),该反应的化学方程式为___。NaBH4与水反应生成NaBO2和H2,该反应生成的氧化产物与还原产物的物质的量之比为___。
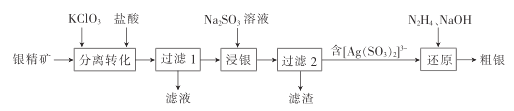
(2)工业上以铁硼矿(主要成分为Mg2B2O5·H2O,还有少量Fe2O3、FeO、CaO、Al2O3和SiO2等)为原料制备单质B的工艺流程如图所示:
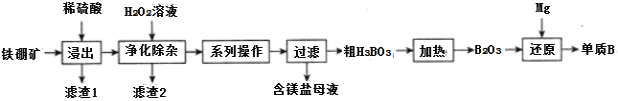
已知:
金属离子 | Fe3+ | Al3+ |
开始沉淀的PH | 2.7 | 3.1 |
沉淀完全的PH | 3.7 | 4.9 |
![]() “浸出”时,将铁硼矿石粉碎的目的为___。
“浸出”时,将铁硼矿石粉碎的目的为___。
![]() 滤渣1的主要成分为___。
滤渣1的主要成分为___。
![]() “净化除杂”时需先加H2O2溶液,其目的为___,然后再调节溶液的pH≈5.0的目的是___。
“净化除杂”时需先加H2O2溶液,其目的为___,然后再调节溶液的pH≈5.0的目的是___。
![]() 制得的粗硼在一定条件下能生成BI3,BI3加热分解可以得到纯净的单质硼。现将0.025g粗硼制成的BI3完全分解,生成的I2用0.30mol·L-1Na2S2O3溶液滴定(I2+2S2O32-=2I-+S4O62-)至终点,消耗18.00mLNa2S2O3溶液。盛装Na2S2O3溶液应用___(填“酸式”或“碱式”)滴定管,该粗硼样品的纯度为___。
制得的粗硼在一定条件下能生成BI3,BI3加热分解可以得到纯净的单质硼。现将0.025g粗硼制成的BI3完全分解,生成的I2用0.30mol·L-1Na2S2O3溶液滴定(I2+2S2O32-=2I-+S4O62-)至终点,消耗18.00mLNa2S2O3溶液。盛装Na2S2O3溶液应用___(填“酸式”或“碱式”)滴定管,该粗硼样品的纯度为___。
【答案】+3 4NaH+B(OCH3)3=NaBH4+3CH3ONa 1:1 增大接触面积,加快反应速率 SiO2、CaSO4 将其中的![]() 氧化为
氧化为![]() 使Fe3+转化为Fe(OH)3沉淀、Al3+转化为Al(OH)3沉淀而除去 碱式 77.8%
使Fe3+转化为Fe(OH)3沉淀、Al3+转化为Al(OH)3沉淀而除去 碱式 77.8%
【解析】
(1)①根据化合价代数和为0,得出B为化合价;
②工业上可利用硼酸甲酯B(OCH3)3与氢化钠NaH反应制备NaBH4,反应的另一种产物为甲醇钠(CH3ONa),该反应的化学方程式为4NaH+B(OCH3)3=NaBH4+3CH3ONa;NaBH4与水反应生成NaBO2和H2,NaBH4+2H2O=NaBO2+4H2↑,NaBH4中H被氧化,得到氧化产物,水中氢被还原,得到还原产物;
(2)以铁硼矿(主要成分为Mg2B2O5·H2O和Fe3O4,还有少量Fe2O3、FeO、CaO、Al2O3和SiO2等)为原料制备硼酸(H3BO3),由流程可知,加硫酸溶解只有SiO2不溶,Mg2B2O5·H2O+2H2SO4=2H3BO3+2MgSO4,CaO转化为微溶于水的CaSO4,“净化除杂”需先加H2O2溶液,将亚铁离子转化为铁离子,调节溶液的pH约为5,使铁离子、铝离子均转化为沉淀,则滤渣为氢氧化铝、氢氧化铁,然后蒸发浓缩、冷却结晶、过滤分离出H3BO3。
(1)①NaBH4中Na是+1价,H是-1价,则B元素的化合价,根据化合价代数和为0,得出B为+3价;
②工业上可利用硼酸甲酯B(OCH3)3与氢化钠NaH反应制备NaBH4,反应的另一种产物为甲醇钠(CH3ONa),该反应的化学方程式为4NaH+B(OCH3)3=NaBH4+3CH3ONa;NaBH4与水反应生成NaBO2和H2,NaBH4+2H2O=NaBO2+4H2↑,NaBH4中H被氧化,得到氧化产物,水中氢被还原,得到还原产物,该反应生成的氧化产物与还原产物的物质的量之比为1:1,故答案为:4NaH+B(OCH3)3=NaBH4+3CH3ONa;1:1;
(2)①“浸出”时,将铁硼矿石粉碎的目的为增大接触面积,加快反应速率,故答案为:增大接触面积,加快反应速率;
②加硫酸溶解只有SiO2不溶,Mg2B2O5·H2O+2H2SO4=2H3BO3+2MgSO4,CaO转化为微溶于水的CaSO4,利用Fe3O4的磁性,可将其从“浸渣”中分离。“浸渣”中还剩余的物质是SiO2、CaSO4,滤渣1的主要成分为SiO2、CaSO4,故答案为:SiO2、CaSO4;
③“净化除杂”需先加H2O2溶液,其目的为将其中的![]() 氧化为
氧化为![]() ,然后再调节溶液的pH≈5.0的目的是使Fe3+转化为Fe(OH)3沉淀、Al3+转化为Al(OH)3沉淀而除去,故答案为:将其中的
,然后再调节溶液的pH≈5.0的目的是使Fe3+转化为Fe(OH)3沉淀、Al3+转化为Al(OH)3沉淀而除去,故答案为:将其中的![]() 氧化为
氧化为![]() ;使Fe3+转化为Fe(OH)3沉淀、Al3+转化为Al(OH)3沉淀而除去;
;使Fe3+转化为Fe(OH)3沉淀、Al3+转化为Al(OH)3沉淀而除去;
![]() I2~3S2O32-,则n(B)=
I2~3S2O32-,则n(B)=![]() n(S2O32-)=0.0018mol,硼的质量为:10.81g·mol-1×0.0018mol=0.01944g,粗硼中硼的含量为:
n(S2O32-)=0.0018mol,硼的质量为:10.81g·mol-1×0.0018mol=0.01944g,粗硼中硼的含量为:![]() ×100%=77.8%,故答案为:碱式;77.8%。
×100%=77.8%,故答案为:碱式;77.8%。

 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案