题目内容
【题目】胆矾CuSO4·5H2O可写[Cu(H2O)4]SO4·H2O,其结构示意图如下:
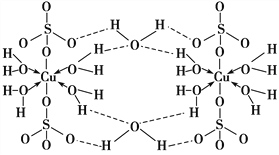
下列有关胆矾的说法正确的是( )
A. 所有氧原子都采取sp3杂化 B. 氧原子参与形成配位键和氢键两种化学键
C. Cu2+的价电子排布式为3d84s1 D. 胆矾中的水在不同温度下会分步失去
【答案】D
【解析】A项,胆矾中H2O中O原子形成2个σ键,O上还有两对孤电子对,H2O中O原子都采取sp3杂化,SO42-中端点氧不发生杂化,A项错误;B项,根据胆矾的结构示意图,氧原子形成极性键、配位键和氢键,氢键不属于化学键,B项错误;C项,基态Cu原子的核外电子排布式为1s22s22p63s23p63d104s1,Cu2+的核外电子排布式为1s22s22p63s23p63d9,Cu2+的价电子排布式为3d9,C项错误;D项,根据胆矾的结构和胆矾可写成[Cu(H2O)4]SO4·H2O,胆矾晶体中水分子有:(1)与Cu2+形成配位键的水分子、(2)与SO42-和配体水分子形成氢键的水分子,由于作用力的不同,胆矾中的水在不同温度下会分步失去,D项正确;答案选D。

练习册系列答案
相关题目