题目内容
【题目】某反应为:NaClO+Cr2(SO4)3+NaOH═Na2CrO4+Na2SO4+NaCl+H2O
(1)配平上述方程式;用双线桥标出该反应中电子转移的方向和数目.
(2)反应中还原剂是(填化学式),被还原的元素是(填元素符号).
【答案】
(1)3|1|10|2|3|3|5| 
(2)Cr2(SO4)3; Cl
【解析】解:(1)反应中氯元素化合价+1价变化为﹣1价,电子转移2e﹣,铬元素化合价+3价变化为+6价,电子转移3e﹣,电子转移总数为6e﹣,NaClO、NaCl前系数乘3,硫酸铬前系数为1,Na2CrO4前系数为2,Na2SO4前系数为3,钠守恒得到NaOH前系数为10,氢元素守恒得到H2O前系数为5,得到配平的化学方程式为:
3NaClO+1Cr2(SO4)3+10NaOH=2Na2CrO4+3Na2SO4+3NaCl+5H2O
电子转移总数6e﹣,双线桥标注电子转移方向和数目得到:

所以答案是:2、1、10、2、3、3、5; 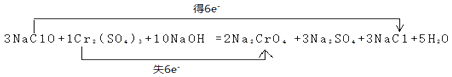 ;(2)3NaClO+1Cr2(SO4)3+10NaOH=2Na2CrO4+3Na2SO4+3NaCl+5H2O,反应中氯元素化合价降低被还原,硫酸铬中个元素化合价升高失电子做还原剂,
;(2)3NaClO+1Cr2(SO4)3+10NaOH=2Na2CrO4+3Na2SO4+3NaCl+5H2O,反应中氯元素化合价降低被还原,硫酸铬中个元素化合价升高失电子做还原剂,
所以答案是:Cr2(SO4)3; Cl.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
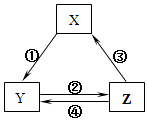
【题目】表所列各组物质中,物质之间通过一步反应就能实现如图所示转化且所给反应条件正确的是( )
选项 | X | Y | Z | 箭头上所标数字的反应条件 |
A | SiO2 | Na2SiO3 | H2SiO3 | ①与Na2CO3熔融 |
B | Na | Na2O2 | NaCl | ②加H2O |
C | NO | NO2 | HNO3 | ③与C加热 |
D | Al2O3 | NaAlO2 | Al(OH)3 | ④与NaOH |
A.A
B.B
C.C
D.D

