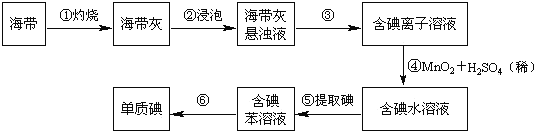
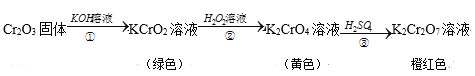
题目内容
【题目】某干燥粉末可能由![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 中的一种或几种组成。将该粉末与足量的盐酸反应有气体
中的一种或几种组成。将该粉末与足量的盐酸反应有气体![]() 逸出,
逸出,![]() 通过足量的
通过足量的![]() 溶液后体积缩小(同温、同压下测定)。若将原来混合粉末在空气中用酒精灯加热,也有气体放出,且剩余固体的质量大于原混合粉末的质量。下列判断正确的是
溶液后体积缩小(同温、同压下测定)。若将原来混合粉末在空气中用酒精灯加热,也有气体放出,且剩余固体的质量大于原混合粉末的质量。下列判断正确的是
①粉末中一定有![]() 、
、![]() 、
、![]() , ②粉末中一定不含
, ②粉末中一定不含![]() 和
和![]()
③粉末中一定不含有![]() 和
和![]() ④无法肯定粉末中是否含有
④无法肯定粉末中是否含有![]() 和
和![]()
A.①④B.②③C.③④D.①②
【答案】A
【解析】
将该粉末与足量的盐酸反应有气体X逸出,X通过足量的NaOH溶液后体积缩小(同温、同压下测定),说明气体中含有二氧化碳,从而得出该粉末中有碳酸钠或碳酸氢钠或两者都有,气体体积缩小,即还剩余有气体,说明剩余气体为氧气,从而说明有过氧化钠;
将原来混合粉末在空气中用酒精灯加热,也有气体放出,只有碳酸氢钠受热要分解,说明一定有碳酸氢钠,
剩余固体的质量大于原混合粉末的质量,说明此固体中有氧化钠,氧化钠在加热时要变为过氧化钠,从而质量增加。
因此得出粉末中一定有氧化钠、过氧化钠、碳酸氢钠,碳酸钠、氯化钠无法确定。故A正确;
答案为A。

【题目】为达到实验目的,下列选用的装置、实验操作均正确的是
实验目的 | 实验步骤和装置 | |
A | 比较H2O2和Fe3+的氧化性 | 将盐酸酸化的双氧水滴入Fe(NO3)2溶液中 |
B | 配制100 mL 1.0 mol·L-1NaOH溶液 | 向100mL容量瓶中加入4.0 g NaOH固体,加水到刻度线 |
C | 验证牺牲阳极的阴极保护法 |
往铁电极附近滴加铁氰化钾溶液 |
D | 探究温度对反应速率的影响 | 将两片大小相同的淀粉碘化钾试纸分别放置于两支规格相同的试管中,向试纸上滴加2.0 mol·L-1的H2SO4溶液2~3滴,密封试管,分别在室温和40℃水浴中反应,观察并记录变色时间 |
A.AB.BC.CD.D
【题目】25 ℃时,部分物质的电离常数如下表所示:
化学式 | CH3COOH | H2C2O4 | H2S |
电离常数 | 1.8×10-5 | Ka1=5.4×10-2 Ka2=5.4×10-5 | Ka1=1.0×10-7 Ka2=7.1×10-15 |
请回答下列问题:
(1)若把CH3COOH、H2C2O4、HC2O4-、H2S、HS- 都看作是酸,其中酸性最弱的是________。
(2)CH3COOH、H2C2O4、H2S的酸性由强到弱的顺序为_____________________。
(3)NaHS溶液与NaHC2O4溶液反应的离子方程式为_______________。
(4)0.1 mol·L-1H2S溶液中c(H+)=________ mol·L-1。
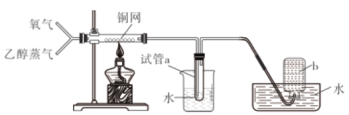
【题目】有关下图所示实验的预测现象不正确的是
选项 | 操作 | 预测现象 |
A | 通入一段时间的氧气后点燃酒精灯 | 铜网会逐渐变黑 |
B | 通入氧气并加热一段时间后通入乙醇蒸气 | 铜网将逐渐变成红色 |
C | 预先通入氧气排净装置中的空气后再进行实验 | 集气瓶b中不会收集到气体 |
D | 观察试管a中收集到的溶液 | 溶液无色有刺激性气味 |
A.AB.BC.CD.D