题目内容
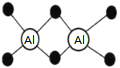
【题目】已知Al2H6燃烧热极高,是一种很好的生氢剂,它跟水反应生成H2,球棍模型如图(白球为Al,黑球为H)。下列推测肯定不正确的是
A. 该物质与水反应,属于氧化还原反应
B. Al2H6分子中氢为+1价,铝为﹣3价
C. Al2H6在空气中完全燃烧,产物为氧化铝和水
D. 氢铝化合物可能成为未来的储氢材料和火箭燃料
【答案】B
【解析】
A.Al2H6与水反应生成氢氧化铝和氢气,该反应中H元素化合价由-1价、+1价变为0价;B.根据元素的电负性和铝的化合价判断;C.根据元素守恒分析; D.根据氢铝化合物的性质分析。
A.Al2H6与水反应生成氢氧化铝和氢气,该反应中H元素化合价由-1价、+1价变为0价,所以属于氧化还原反应,选项A正确;B.在化合物中电负性大的显负价,电负性小的元素显正价,氢元素的电负性大于铝元素,氢铝化合物中铝元素显+3价,氢元素显-1价,选项B错误; C.根据题中信息Al2H6的燃烧热极高,判断Al2H6能燃烧,根据原子守恒,Al2H6的组成元素只有Al、H两种元素,又由于是在氧气中燃烧,推出燃烧产物为氧化铝和水,选项C正确;D.氢铝化合物能和水反应生成氢氧化铝和氢气,可以作储氢材料,燃烧热极高可以作火箭燃料,选项D正确。答案选B。

 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案【题目】生产液晶显示器过程中使用的化学清洗剂NF3是一种温室气体,其存储能量的能力是CO2的12000-20000倍,在大气中的寿命可长达740年之久,以下是几种化学键的键能:
化学键 |
|
|
|
键能 | 941.7 | 154.8 | 283.0 |
下列说法中正确的是( )
A. 反应中![]() 为吸热反应
为吸热反应
B. 过程![]() 放出能量
放出能量
C. 反应中![]() ,N2与F2的总能量小于NF3的总能量
,N2与F2的总能量小于NF3的总能量
D. NF3吸收能量后如果没有化学键的断裂与生成,仍可能发生化学反应
【题目】下列实验中的颜色变化,与氧化还原反应无关的是
选项 | A | B | C | D |
实验 | NaOH溶液滴入FeSO4溶液中 | 石蕊溶液滴入氯水中 | KSCN溶液滴入FeCl3溶液中 | CO2通过装有Na2O2固体的干燥管 |
现象 | 产生白色沉淀,随后变为红褐色 | 溶液变红,随后迅速褪色 | 溶液变为红色 | 固体由淡黄色变为白色 |
A. A B. B C. C D. D
