题目内容
2.将下列各组中的每种有机物放入水中,振荡后再静置,液体分层且该组的全部物质都能浮在水的上层的是( )| A. | 乙酸乙酯、甲苯、十一烷 | B. | 乙醇、苯、庚烯 | ||
| C. | 甘油、甲醛、硝基苯 | D. | 溴苯、四氯化碳、苯磺酸钠 |
分析 有机物放入水中,振荡后静置,能分层且浮于水面上,说明该物质不溶于水,且密度比水小,以此来解答即可.
解答 解:A、乙酸乙酯、甲苯以及十一烷均不溶于水,且密度比水小,混合后浮于水面上,故A正确;
B、乙醇与水互溶,溶液不分层,故B错误;
C、甘油和甲醛均能溶于水,故C错误;
D、苯磺酸钠为盐,能溶于水,故D错误,
故选A.
点评 本题主要考查的是常见有机物的物理性质,把握物质的性质为解答的关键,侧重分液及物质密度的考查,注意常见有机物的溶解性,题目难度不大.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
6.25mL的盐酸溶液中加入4g氢氧化钠恰好中和,若改用氢氧化钡中和需要( )
| A. | 17.1g | B. | 8.55g | C. | 34.2g | D. | 3.4g |
13.下列说法正确的是( )
| A. | 化学反应进行的越快,化学反应现象越明显 | |
| B. | 某反应中,经2min后B浓度减少0.6mol•L-1,在2min时用B表示的反应速率为0.6mol•L-1•min | |
| C. | 化学反应中的能量变化都是化学能转化成热能 | |
| D. | 原电池的反应一定是氧化还原反应 |
10.草酸(H2C2O4)是一种重要的有机化工原料.为探究草酸的性质,某化学研究性学习小组查阅了有关资料,有关物质的部分性质如下表:
【实验Ⅰ】
探究草酸的不稳定性.用下图中提供的仪器和试剂,验证草酸受热分解得到的混合气体中含有CO和CO2(加热装置和导管等在图中略去,部分装置可以重复使用).
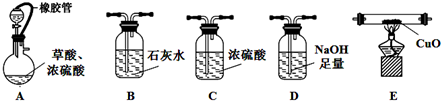
(1)仪器装置正确连接顺序为:ABDCEB.
(2)用上图入提供的装置和试剂实验时,在B中观察到有白色沉淀,也不能说明草酸分解有CO2,请提也改进意见在A与B之间添加一个盛水的洗气瓶,除去草酸蒸气(或在烧瓶上连接冷凝管).
【实验Ⅱ】
实验室用硝酸氧化淀粉水解液法制备草酸.装置如下图所示,反应原理为:
C6H12O6+12HNO3=3H2C2O4+9NO2↑+3NO↑+9H2O
实验步骤如下:
①一定量的淀粉水解液加入三颈烧瓶中
②控制反应温度55-60℃,边搅拌边缓慢滴加一定量的混合酸(65%的HNO3与98%的H2SO4的质量比2:1.25)
③反应3小时,蒸发浓缩、冷却结晶,抽滤后再重结晶得到草酸晶体
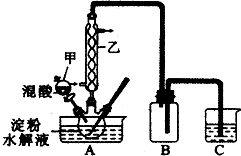
(3)上图实验装置中仪器乙的名称为:冷凝管、装置B的作用安全瓶,防止倒吸、C中试剂是NaOH溶液.
(4)检验淀粉是否水解完全的操作及现像是:取适量水解液于试管中,加入碘水,若溶液变蓝则淀粉水解完全,若溶液不变蓝则淀粉水解不完全.
【实验Ⅲ】
制备草酸亚铁晶体(FeC2O4•2H2O).反应原理为:
FeSO4•(NH4)2SO4•6H2O+H2C2O4=FeC2O4•2H2O+(NH4)2SO4+H2SO4+4H2O
实验步骤如下:
①称取13.7g FeSO4•(NH4)2SO4•6H2O放在200mL烧杯中,然后加30mL蒸馏水和2mL 2mol•L-1 H2SO4,加热溶解.
②再加入40mL 1mol•L-1草酸溶液,加热至沸,然后迅速搅拌(防止暴沸),待有黄色晶体析出后,停止加热,静置.
③弃去上层清液,用40mL蒸馏水充分洗涤晶体,过滤后,再用丙酮洗涤晶体并晾干得4.6g FeC2O4•2H2O
(5)生成的FeC2O4•2H2O需要充分洗涤,检验是否洗涤干净的操作及现像是用小试管取少量最后一次洗涤液,加入BaCl2溶液,如出现白色沉淀,说明沉淀没有洗涤干净,否则,沉淀已洗涤干净.
(6)用丙酮洗涤晶体的目的是减少草酸亚铁晶体的溶解,更快除去草酸亚铁晶体表面的水分.
(7)本实验FeC2O4•2H2O的产率为73.1%.
| 物质 | 物理性质 | 化学性质 |
| 草酸(H2C2O4) | ①易溶于水 ②熔点189.5℃、100℃开始升华 ③草酸钙和草酸氢钙均是白色不溶物 | ①二元弱酸、酸性比碳酸强 ②有毒、具有腐蚀性 ③157℃左右分解、与浓硫酸混合会产生H2O、CO和CO2 |
| 草酸亚铁晶体(FeC2O4•2H2O) | ①浅黄色粉末状晶体 ②微溶于水,难溶于丙酮 | 受热易分解为氧化亚铁或铁单质 |
| 丙酮 | 与水互溶、易挥发 | ---- |
探究草酸的不稳定性.用下图中提供的仪器和试剂,验证草酸受热分解得到的混合气体中含有CO和CO2(加热装置和导管等在图中略去,部分装置可以重复使用).

(1)仪器装置正确连接顺序为:ABDCEB.
(2)用上图入提供的装置和试剂实验时,在B中观察到有白色沉淀,也不能说明草酸分解有CO2,请提也改进意见在A与B之间添加一个盛水的洗气瓶,除去草酸蒸气(或在烧瓶上连接冷凝管).
【实验Ⅱ】
实验室用硝酸氧化淀粉水解液法制备草酸.装置如下图所示,反应原理为:
C6H12O6+12HNO3=3H2C2O4+9NO2↑+3NO↑+9H2O
实验步骤如下:
①一定量的淀粉水解液加入三颈烧瓶中
②控制反应温度55-60℃,边搅拌边缓慢滴加一定量的混合酸(65%的HNO3与98%的H2SO4的质量比2:1.25)
③反应3小时,蒸发浓缩、冷却结晶,抽滤后再重结晶得到草酸晶体

(3)上图实验装置中仪器乙的名称为:冷凝管、装置B的作用安全瓶,防止倒吸、C中试剂是NaOH溶液.
(4)检验淀粉是否水解完全的操作及现像是:取适量水解液于试管中,加入碘水,若溶液变蓝则淀粉水解完全,若溶液不变蓝则淀粉水解不完全.
【实验Ⅲ】
制备草酸亚铁晶体(FeC2O4•2H2O).反应原理为:
FeSO4•(NH4)2SO4•6H2O+H2C2O4=FeC2O4•2H2O+(NH4)2SO4+H2SO4+4H2O
实验步骤如下:
①称取13.7g FeSO4•(NH4)2SO4•6H2O放在200mL烧杯中,然后加30mL蒸馏水和2mL 2mol•L-1 H2SO4,加热溶解.
②再加入40mL 1mol•L-1草酸溶液,加热至沸,然后迅速搅拌(防止暴沸),待有黄色晶体析出后,停止加热,静置.
③弃去上层清液,用40mL蒸馏水充分洗涤晶体,过滤后,再用丙酮洗涤晶体并晾干得4.6g FeC2O4•2H2O
(5)生成的FeC2O4•2H2O需要充分洗涤,检验是否洗涤干净的操作及现像是用小试管取少量最后一次洗涤液,加入BaCl2溶液,如出现白色沉淀,说明沉淀没有洗涤干净,否则,沉淀已洗涤干净.
(6)用丙酮洗涤晶体的目的是减少草酸亚铁晶体的溶解,更快除去草酸亚铁晶体表面的水分.
(7)本实验FeC2O4•2H2O的产率为73.1%.
17.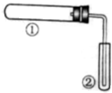 用如图装置(夹持、加热装置已略)进行实验,有②中现象,不能证实①中反应发生的是( )
用如图装置(夹持、加热装置已略)进行实验,有②中现象,不能证实①中反应发生的是( )
 用如图装置(夹持、加热装置已略)进行实验,有②中现象,不能证实①中反应发生的是( )
用如图装置(夹持、加热装置已略)进行实验,有②中现象,不能证实①中反应发生的是( )| ①中实验 | ②中现象 | |
| Ⅰ | 铁粉与水蒸气加热 | 肥皂水冒泡 |
| Ⅱ | 加热NH4Cl和Ca(OH)2混合物 | 酚酞溶液变红 |
| Ⅲ | NaHCO3 | 澄清石灰水变浑浊 |
| A. | 只有Ⅰ | B. | 只有Ⅱ | ||
| C. | 只有Ⅲ | D. | Ⅰ、Ⅱ、Ⅲ均能证实①中反应发生 |
7.在①硫酸②重晶石③三氧化硫④绿矾四种化合物中,硫元素的质量分数由高到底排列的顺序是( )
| A. | ①>②>③>④ | B. | ②>③>④>① | C. | ①>③>②>④ | D. | ③>①>②>④ |
14.下列物质属于单质的是( )
| A. | CH4 | B. | NaCl | C. | H2SO4 | D. | O2 |
12.下列用连线方法对部分化学知识进行归纳的内容中,有错误的组是( )
| A. | 物质的性质与用途: 磺胺类药物能抑制细菌合成核酸--治疗肺炎、脑膜炎、尿路感染、呼吸道感染 酸能与碱中和-----胃酸过多的病人服用含氢氧化镁的药物 | |
| B. | 保护环境: 控制“白色污染”--禁止使用所有塑料制品 防止水的污染--提倡使用无磷洗衣粉 | |
| C. | 基本安全常识: 饮用假酒中毒--由甲醇引起 食用假盐中毒--由亚硝酸钠引起 | |
| D. | 生活中的一些做法: 除去衣服上的油污--可用汽油洗涤 使煤燃烧更旺--可增大煤与空气接触面积 |