题目内容
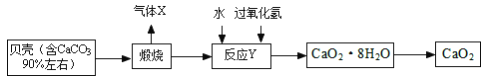
【题目】二氧化铈(CeO2)是一种主要的稀土氧化物。平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2以及其他少量可溶于稀酸的物质)。某课题组就此粉末为原料回收铈,设计实验流程如下:
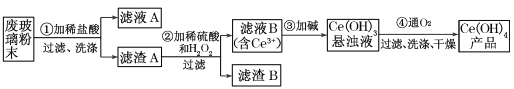
(1)洗涤滤渣A的目的是为了除去_____________(填离子符号),检验该离子是否洗净的方法是________________。
(2)第②步反应的离子方程式是___________________,滤渣B的主要成分是___________。
(3)萃取是分离稀士元素的常用方法,已知化合物TBP作为萃取剂能将铈离子从水溶液中萃取出来,TBP_______(填“能”或“不能”)与水互溶。实验室进行萃取操作时用到的主要玻璃仪器有___________、烧杯、玻璃棒、量筒等。
(4)取上述流程中得到的Ce(OH)4产品0.536 g,加硫酸溶解后,用0.1000 mol·L-1FeSO4标准溶液滴定至终点时(铈被还原为Ce3+),消耗25.00 mL标准维液,该产品中Ce(OH)4的质量分数为_______________(保留3位有效数字)
【答案】 Fe3+、Cl— 取最后洗涤液少量于试管中,滴加几滴AgNO3溶液,如无白色沉淀,则洗干净(或取最后洗涤液少量于试管中,滴加几滴KSCN溶液,若溶液不变血红色,则洗干净) 2CeO2+H2O2+6H+=2Ce3++O2↑+4H2O SiO2 不能 分液漏斗 97.0%
【解析】(1)滤渣A上含有FeCl3,洗涤滤渣A的目的是为了除去Fe3+、Cl-,因此检验是否洗涤干净的实验操作为:取最后一次洗涤液,加入KSCN溶液,若不出现红色,则已洗净,反之,未洗净或取最后洗涤液少量,滴加AgNO3,如无白色沉淀,则洗干净;(2)稀硫酸、H2O2,CeO2三者反应生成转化为Ce2(SO4)3、O2和H2O,反应的离子方程式为:2CeO2+H2O2+6H+=2Ce3++O2↑+4H2O;加入稀硫酸和H2O2,CeO2转化为Ce3+,SiO2不反应,滤渣B的成分为SiO2;(3)化合物TBP作为萃取剂能将铈离子从水溶液中萃取出来,所以TBP不能与水互溶,实验室进行萃取操作时用到的主要玻璃仪器有分液漏斗、烧杯、玻璃棒、量筒等;(4)用0.1000mol/LFeSO4溶液滴定至终点,铈被还原成Ce3+,则Fe2+被氧化为Fe3+,则
Ce(OH)4~FeSO4
0.0025mol 0.1000mol/L-1×0.025L
所以m[Ce(OH)4]=0.0025mol×208g/mol=0.52g
产品中Ce(OH)4的质量分数为0.52/0.536×100%=97.0%。

 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案