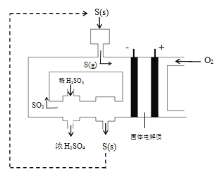
题目内容
【题目】在容积为1 L的容器中,通入一定量的N2O4,发生反应N2O4(g)![]() 2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
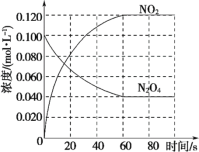
(1)反应的ΔH_____0(填“大于”或“小于”);100 ℃时,体系中各物质浓度随时间变化如图所示。在 0~60 s 时段, 反应速率 v(N2O4)为_____mol·L-1·s-1;反应的平衡转化率为:_____; 反应的平衡常数K1为_____。
(2)100℃时达平衡后,改变反应温度为 T,N2O4以0.002 0 mol·L-1·s-1的平均速率降低,经10 s又达到平衡。
a:T____________100℃(填“大于”或“小于”),判断理由是__________。
b:计算温度T时反应的平衡常数K2____________。
(3)温度T时反应达平衡后,将反应容器的容积减少一半。平衡向____________(填“正反应”或“逆反应”)方向移动,判断理由________________________。
【答案】大于 0.0010 60% 0.36 大于 温度改变后,反应正向移动,由于正反应为吸热反应,所以温度改变是升高温度 1.28 逆反应 对于气体分子数增大的反应,增大压强平衡向逆反应方向移动
【解析】
(1)升高温度混合气体颜色变深,说明升高温度,化学平衡正向移动,利用温度对化学平衡移动的影响分析判断反应的热效应;在0~60 s时段,根据v=![]() 计算反应速率;根据反应物的转化率=
计算反应速率;根据反应物的转化率=![]() ×100%计算N2O4的转化率;根据化学平衡常数K1=
×100%计算N2O4的转化率;根据化学平衡常数K1=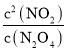 计算平衡常数;
计算平衡常数;
(2)根据温度对化学反应速率的影响分析判断;计算在反应达到新的平衡后各种物质的浓度,带入平衡常数表达式计算出新平衡的化学平衡常数K2;
(3)温度T时反应达到平衡后,将反应容器的容积减少一半,相当于增大压强,根据压强对化学平衡移动的影响分析判断。
(1)升高温度混合气体颜色变深,说明升高温度,化学平衡正向移动,根据平衡移动原理:升高温度,化学平衡向吸热反应方向移动,则该反应的正反应为吸热反应,故△H>0;在0~60 s时段,反应速率v(N2O4)=![]() =0.0010 mol/(L·s);反应中N2O4的平衡转化率=
=0.0010 mol/(L·s);反应中N2O4的平衡转化率=![]() ×100%=60%;达到平衡时c(N2O4)=0.040 mol/L、c(NO2)=0.120 mol/L,化学平衡常数K1=
×100%=60%;达到平衡时c(N2O4)=0.040 mol/L、c(NO2)=0.120 mol/L,化学平衡常数K1=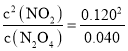 =0.36;
=0.36;
(2)a.在0~60 s时段,反应速率v(N2O4)= 0.001 mol/(L·s)<0.0020 mol/(L·s),可见改变温度后化学反应速率加快,说明改变的温度是升高温度,则T>100℃;
b.根据a知,改变的条件是升高温度,化学平衡正向移动,改变条件后10 s内△c(N2O4)=0.002 0mol/(Ls)×10 s=0.020 mol/L,则再次达到平衡时c(N2O4)=(0.040-0.020)mol/L=0.020 mol/L,c(NO2)=(0.120+0.020×2)mol/L=0.160 mol/L,所以在温度T时反应的平衡常数K2= K1=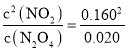 =1.28;
=1.28;
(3)在温度T时,反应达到平衡后,将反应容器的容积减小一半,相当于增大体系的压强,由于该反应的正反应为气体体积增大的反应,所以增大压强,化学平衡向气体体积减小的方向移动,即化学平衡向逆反应方向移动。

 期末集结号系列答案
期末集结号系列答案