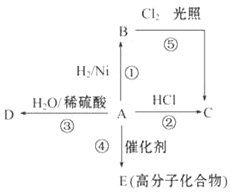
题目内容
【题目】对剧毒的氰化物可在碱性条件下用如下方法进行处理:2CN—+8OH—+5Cl2 = 2CO2+N2+10Cl—+4H2O。下列判断正确的是 ( )
A. 当有0.2mol CO2生成时,溶液中阴离子的物质的量增加![]()
B. 该反应中,每有2molCN—反应,转移电子为![]()
C. 上述反应中的还原剂是![]()
D. 还原性:Cl—>CN—
【答案】B
【解析】试题分析:根据方程式可知,反应中碳元素的化合价从+2升高到+4价,失去2个电子。氮元素的化合价从-3价升高到0价,失去3个电子,因此CN-是还原剂;氯元素的化合价从0价降低到-1价,得到1个电子,氯气是氧化剂。A、根据方程式可知,反应前后溶液中阴离子的个数是不变,A不正确;B、该反应中,每有2molCN-反应,转移电子为2mol×5=10mol,B正确;C、还原剂是CN-,C不正确;D、氧化还原反应中还原剂的还原性强于还原产物的还原性,所以还原性是CN->C1-,D不正确,答案选B。

练习册系列答案
相关题目
【题目】根据下列实验或实验操作和现象,所得结论正确的是
实验或实验操作 | 现象 | 实验结论 | |
A | 用大理石和盐酸反应制取CO2气体,立即通入一定浓度的Na2SiO3溶液中 | 出现白色沉淀 | H2CO3的酸性比H2SiO3的酸性强 |
B | 向某溶液先滴加硝酸酸化,再滴加BaCl2溶液 | 有白色沉淀生成 | 原溶液中含有SO42-、SO32-、HSO3-中的一种或几种 |
C |
| 试管b比试管a中溶液的红色深 | 增大反应物浓度,平衡向正反应方向移动 |
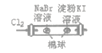
D |
| 左边棉球变为橙色,右边棉球变为蓝色 | 氧化性:Cl2>Br2>I2 |
A. A B. B C. C D. D