题目内容
绿矾(FeSO4·7H2O)是治疗缺铁性贫血药品的重要成分。下面是以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法:
已知:室温下饱和H2S溶液的pH约为3.9,SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5。
(1)检验制得的绿矾晶体中是否含有Fe3+的实验操作是______________________________。
(2)操作II中,通入硫化氢至饱和的目的是 ;在溶液中用硫酸酸化至pH=2的目的是 。
(3)操作IV的顺序依次为: 、 ___、 。
操作IV得到的绿矾晶体用少量冰水洗涤,其目的是:①除去晶体表面附着的硫酸等杂质;② 。
(4)测定绿矾产品中Fe2+含量的方法是:a.称取2.8500g绿矾产品,溶解,在250mL容量瓶中定容;b.量取25.00mL待测溶液于锥形瓶中;c.用硫酸酸化的0.01000mol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL(滴定时发生反应的离子方程式为:5Fe2++MnO4¯+8H+→5Fe3++Mn2++4H2O)。
①判断此滴定实验达到终点的方法是 。
②计算上述样品中FeSO4·7H2O的质量分数为 _(用小数表示,保留三位小数)。
(1)取少量晶体溶于水,滴加KSCN溶液,若溶液不显现红色,表明溶液不含Fe3+(1分)
(2)除去溶液中的Sn2+离子,并防止Fe2+被氧化 (2分) 防止Fe2+离子生成沉淀(1分)
(3)蒸发 (1分)冷却结晶 (1分) 过滤(1分)②降低洗涤过程中FeSO4·7H2O的损耗(1分)
(4)①滴加最后一滴KMnO4溶液时,溶液变成浅红色且半分钟内不褪色。(2分)
② 0.975 (2分)
解析试题分析:(1)检验Fe3+一般用敏感试剂KSCN溶液,方法为取少量晶体溶于水,滴加KSCN溶液,若溶液不显现红色,表明溶液不含Fe3+;
(2)通入硫化氢是为了除去杂质锡离子,同时硫化氢具有较强的还原性防止亚铁离子被氧化;FeS开始沉淀时溶液的pH为3.0,故酸化至pH=2是防止Fe2+离子生成沉淀(室温下饱和H2S溶液的pH约为3.9);
(3)从滤液中得到绿矾晶体,应采用降温结晶的方法,具体为蒸发浓缩、冷却结晶,过滤得到晶体;用洗涤的主要作用是除去表面杂质,少量冰水洗涤是降低晶体溶解,减少溶解损失;
(4)高锰酸钾溶液有颜色,可以根据颜色变化确定反应进行的程度;
根据方程式找出关系得:n(Fe2+)=5n(MnO4¯)=5×0.01000×20.00×10-3=10-3mol
样品中FeSO4·7H2O的质量分数w=10-3×278÷2.8500=0.975
考点:考查化学实验中定性操作和定量分析有关问题。

 阅读快车系列答案
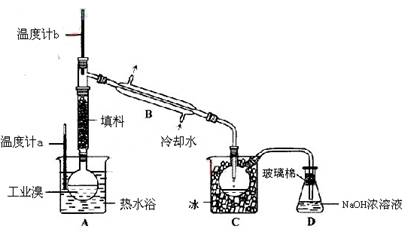
阅读快车系列答案溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
| | 苯 | 溴 | 溴苯 |
| 密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
按下列合成步骤回答问题:
(1)在a中加入15 mL无水苯和少量铁屑。在b中小心加入4.0 mL液态溴。向a中滴入几滴溴,有白色烟雾产生,是因为生成了_______气体。继续滴加至液溴滴完。装置d的作用是_____ ___;
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10 mL水,然后过滤除去未反应的铁屑;
②滤液依次用10 mL水、8 mL 10%的NaOH溶液、10 mL水洗涤。NaOH溶液洗涤的作用是________;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是____________________;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为________,要进一步提纯,下列操作中必需的是________(填入正确选项前的字母);
A.重结晶 B.过滤 C.蒸馏 D.萃取
(4)在该实验中,a的容积最适合的是________ (填入正确选项前的字母)。
A. 25 mL B.50 mL C.250 mL D.500 mL
富马酸亚铁(分子式为C4H2O4Fe,结构简式为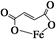 )是一种限量使用的铁强化剂。
)是一种限量使用的铁强化剂。
(1)下图为实验室模拟工业制取富马酸亚铁的流程图: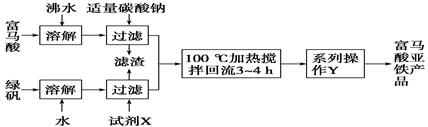
①根据题意,请你写出富马酸的结构简式:________________________。
②绿矾(FeSO4·7H2O)在保存过程中形成的杂质主要有________(填化学式)。
③操作Y包括________、冷却结晶、过滤、洗涤、干燥等。
④判断操作Y中“洗涤”富马酸亚铁产品表明已洗净的实验方法是___________。
(2)设计一个实验方案,证明所得富马酸亚铁产品属于亚铁盐(可供选用的试剂有KSCN溶液、H2O2溶液、稀硫酸。)。填写下表相应空格:
| 步骤 | 实验操作与现象 |
| ① | 取富马酸亚铁产品1.5 g,加入稀硫酸25 mL,用水稀释至50 mL,加热使其完全溶解并反应,冷却后过滤(除去生成的富马酸及可能过量的反应物),保存滤液 |
| ② | |
| ③ | |
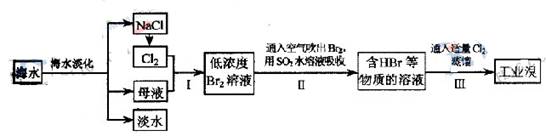
某化学兴趣小组的同学通过以下步骤提取海带中的碘:
①将海带晒干灼烧成灰 ②将海带灰浸泡得其悬浊液 ③过滤得含碘离子的溶液 ④向该溶液中加入适量Cl2置换出碘 ⑤对含碘溶液进行一系列的提取后得碘单质
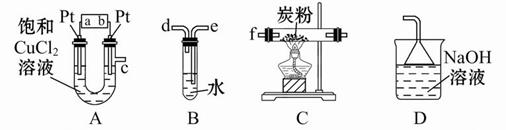
(1)灼烧过程可在下列那种仪器中进行_____________
| A.烧杯 | B.试管 | C.蒸发皿 | D.坩埚 |
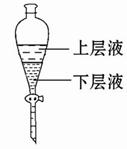
(3)用有机溶剂将碘从水中提取出来需用到下列哪套装置

(4)若用四氯化碳作溶剂进行提取,则分层后下层物质为