题目内容
【题目】【离子反应】某工业废水中仅含下表离子中的5种(不考虑水的电离及离子的水解),且各种离子的物质的量浓度相等,均为0.1mol/L。
阳离子 | K+ Cu2+ Fe3+ Al3+ Fe2+ |
阴离子 | Cl- |
甲同学欲探究废水的组成,进行了如下实验:
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察)。
Ⅱ.取少量溶液,加入KSCN溶液无明显变化。
Ⅲ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类与原溶液中种类相同。
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成。
请推断:
(1) 仅由Ⅰ、Ⅱ判断,溶液中一定不含有的阳离子是___________(写离子符号)
(2) Ⅲ中加入少量盐酸生成无色气体的的离子方程式是______________________
(3) 将Ⅲ中所得红棕色气体通入水中,气体变无色,所发生的化学方程式为____________
(4) 甲同学最终确定原溶液中所含阳离子是___________,阴离子是______________(写
离子符号)
(5) 工业废水中常含有不同类型的污染物,可采用不同的方法处理。以下是乙同学针对含
不同污染物的废水提出的处理措施和方法,其中正确的是__________________。
选项 | 污染物 | 处理措施 | 方法类别 |
A | 废酸 | 加生石灰中和 | 物理法 |
B | Cu2+等重金属离子 | 加硫酸盐沉降 | 化学法 |
C | 含复杂有机物的废水 | 通过微生物代谢 | 物理法 |
D | 碱性的废水 | td style="width:106.85pt; border-top-style:solid; border-top-width:0.75pt; border-right-style:solid; border-right-width:0.75pt; border-left-style:solid; border-left-width:0.75pt; padding-right:5.03pt; padding-left:5.03pt; vertical-align:middle">化学法 |
【答案】(1)K+ Fe3+ (2)3Fe2+ + NO3- + 4H+ = 3Fe3+ + NO + 2H2O(3分)
(3)3NO2+H2O=2HNO3+NO(4)Fe2+ Cu2+ Cl- NO3- SO42-(2分)
(5)D (2分)
【解析】
试题分析:(1)K的焰色呈紫色,透过蓝色钴玻璃观察无紫色火焰,说明没有K+,Fe3+遇KSCN溶液呈血红色,取少量溶液,加入KSCN溶液无明显变化,说明没有Fe3+,所以Ⅰ、Ⅱ判断,溶液中一定不含有的阳离子是K+、Fe3+。
(2))Ⅲ中加入少量盐酸生成无色气体,该无色气体遇空气变成红棕色,说明无色气体是NO,推断溶液中含有NO3-和Fe2+,反应的离子方程式是3Fe2++NO3- +4H+ =3Fe3+ +NO+2H2O。
(3)将Ⅲ中所得红棕色气体通入水中,气体变无色,所发生的化学方程式3NO2+H2O=2HNO3+NO。
(4)若向溶液中加入KSCN溶液,无明显变化,说明原溶液中不含Fe3+;若向溶液中加入过量的盐酸,有气体生成,溶液中阴离子种类不变,说明原溶液中含有Cl-,该气体只能是NO,说明含有具有氧化性的NO3-和还原性的Fe2+,若向溶液中加入BaCl2溶液,有白色沉淀生成,说明原溶液中含有SO42-,各离子的物质的量均为0.1mol,根据电荷守恒可知还应含有Cu2+,所以原溶液中所含阳离子是Fe2+、Cu2+;阴离子是NO3-、Cl-、SO42-。
(5)污染治理要求能除掉有毒的物质,新生成的物质对环境无污染,物理法与化学法的区别是否有新物质生成。A.酸和碱的中和反应为化学反应,为化学法,A项错误;B.硫酸铜可溶,所以不能沉淀除去,B项错误;C.含苯废水中的苯通过微生物代谢,这是化学方法,C项错误;D.碱性的废水与二氧化碳反应生成的碳酸盐和水,无污染,该方法属于化学法,D项正确;答案选D。

 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案【题目】某同学学习了化学反应速率后,联想到曾用H2O2制备氧气,于是设计了下面的实验方案并进行实验探究。
实验编号 | 反 应 物 | 催 化 剂 |
甲 | 试管中加入3 mL 2﹪ H2O2溶液和3滴蒸馏水 | 无 |
乙 | 试管中加入3 mL 5﹪ H2O2溶液和3滴蒸馏水 | 无 |
丙 | 试管中加入3 mL 5﹪ H2O2溶液和3滴蒸馏水 | 1 mL 0.1 mol/L FeCl3溶液 |
丁 | 试管中加入3 mL 5﹪ H2O2溶液和3滴稀盐酸溶液 | 1 mL 0.1 mol/L FeCl3溶液 |
戊 | 试管中加入3 mL 5﹪ H2O2溶液和3滴NaOH溶液 | 1 mL 0.1 mol/L FeCl3溶液 |
【查阅资料】过氧化氢(H2O2),其水溶液俗称双氧水,常温下是一种无色液体,性质比较稳定。在加热的条件下,它能分解生成氧气。研究表明,将新制的5﹪的H2O2溶液加热到65℃时就有氧气放出,加热到80℃时就有较多氧气产生。
(1)上述实验发生反应的化学方程式为 。
(2)实验甲和实验乙的实验目的是 ;
实验丙、实验丁和实验戊的实验目的是 。
(3)请根据该同学查阅的资料分析H2O2的性质,解释实验甲和实验乙能否达到实验目的? 。
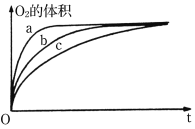
(4)实验过程中该同学对实验丙、丁、戊中产生的气体进行收集,并在2分钟内6个时间点对注射器内气体进行读数,记录数据如下表。
时间/s | 20 | 40 | 60 | 80 | 100 | 120 | |
气体体积/mL | 实验丙 | 9.5 | 19.5 | 29.0 | 36.5 | 46.0 | 54.5 |
实验丁 | 8.0 | 16.0 | 23.5 | 31.5 | 39.0 | 46.5 | |
实验戊 | 15.5 | 30.0 | 44.5 | 58.5 | 71.5 | 83.0 | |
①对实验戊,0~20 s的反应速率v1= mL/s,100~120 s的反应速率v2= mL/s。
不考虑实验测量误差,二者速率存在差异的主要原因是 。
②如右图是根据实验收集到最大体积的气体时所用时间绘制的图像。曲线c表示的是实验 (填“丙”、“丁”或“戊”)。