ЬтФПФкШн
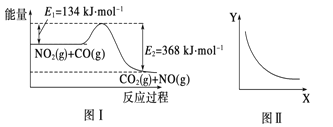
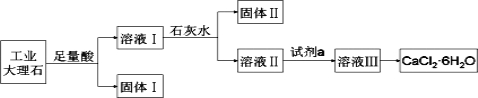
ЁОЬтФПЁПФГЭЌбЇВЩгУЙЄвЕДѓРэЪЏ(КЌгаЩйСПSiO2ЁЂAl2O3ЁЂFe2O3ЕШдгжЪ)жЦШЁCaCl2ЁЄ6H2OЃЌЩшМЦСЫШчЯТСїГЬЃК
ЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ( )
AЃЎЙЬЬхЂёжаКЌгаSiO2ЃЌЙЬЬхЂђжаКЌгаFe(OH)3
BЃЎЪЙгУЪЏЛвЫЎЪБЃЌвЊПижЦpHЃЌЗРжЙЙЬЬхЂђжаAl(OH)3зЊЛЏЮЊAlO2Ѓ
CЃЎДгШмвКЂѓЕУЕНCaCl2ЁЄ6H2OВњЦЗЕФЙ§ГЬжаЃЌаыПижЦКУЬѕМўЗРжЙВњЮяЗжНт
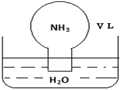
DЃЎШєИФБфЪЕбщЗНАИЃЌдкШмвКЂёжажБНгМгАБЫЎжСГСЕэЭъШЋЃЌТЫШЅГСЕэЃЌЦфШмвКОеєЗЂХЈЫѕЁЂРфШДНсОЇвВПЩЕУЕНДПОЛCaCl2ЁЄ6H2O
ЁОД№АИЁПD
ЁОНтЮіЁП
ЪдЬтЗжЮіЃКЙЄвЕДѓРэЪЏ(КЌгаЩйСПSiO2ЁЂAl2O3ЁЂFe2O3ЕШдгжЪ)МгзуСПЕФбЮЫсЃЌЕУЕНЖўбѕЛЏЙшГСЕэКЭТШЛЏИЦЁЂТШЛЏТСЁЂТШЛЏЬњЛьКЯШмвКЃЌЫљвдЙЬЬхЂёжаКЌгаSiO2ЃЌТЫвКжаМгЪЏЛвЫЎЃЌПижЦpHЃЌПЩвдЕУЕНAl(OH)3ЁЂFe(OH)3ГСЕэЃЌМДЮЊЙЬЬхЂђЃЌЙ§ТЫЃЌЕУТЫвКдйбЮЫсжаИїЙ§СПЕФЧтбѕЛЏИЦЃЌЕУТШЛЏИЦШмвКЃЌCaCl26H2OвзЗжНтЃЌЫљвдДгШмвКжаЛёЕУТШЛЏИЦОЇЬхЪБЃЌвЊЗРжЙЦфЗжНтЁЃAЁЂИљОнЩЯУцЕФЗжЮіПЩжЊЃЌЙЬЬхЂёжаКЌгаSiO2ЃЌЙЬЬхЂђжаКЌгаFe(OH)3ЃЌЙЪAе§ШЗЃЛBЁЂЧтбѕЛЏТСОпгаСНадЃЌПЩШмгкЧтбѕЛЏИЦШмвКЃЌЩњГЩAlO2-ЃЌЙЪBе§ШЗЃЛCЁЂCaCl26H2OвзЗжНтЃЌЫљвдДгШмвКжаЛёЕУТШЛЏИЦОЇЬхЪБЃЌвЊЗРжЙЦфЗжНтЃЌЙЪCе§ШЗЃЛDЁЂШєИФБфЪЕбщЗНАИЃЌдкШмвКЂёжажБНгМгАБЫЎжСГСЕэЭъШЋЃЌТЫШЅГСЕэЃЌЦфШмвКжаКЌгаТШЛЏяЇЃЌОеєЗЂХЈЫѕЁЂРфШДНсОЇЕУЕНЕФCaCl26H2OВЛДПЃЌЙЪDДэЮѓЃЛЙЪбЁDЁЃ

 ЪжРЪжШЋгХСЗПМОэЯЕСаД№АИ
ЪжРЪжШЋгХСЗПМОэЯЕСаД№АИ